میگرن
نقشه یادگیری این مقاله
۱. پادکست: برای درک کلی، ابتدا به پادکست گوش دهید.
۲. ویدیو: ویدیو آموزشی را برای یادگیری عمیق مشاهده کنید.
۳. مطالعه متن: در نهایت، متن مقاله را به عنوان منبع جامع مرور کنید.
مشاهده ویدیو در آپارات
تحلیل جامع مدیریت آستانه میگرن
از پاتوفیزیولوژی ژنتیکی کانالوپاتی تا پروتکلهای بهداشت عصبی و راهبردهای اصلاح سبک زندگی
میگرن به عنوان یکی از پیچیدهترین و ناتوانکنندهترین اختلالات عصبی در سطح جهان شناخته میشود که فراتر از یک سردرد ساده، مجموعهای از فعل و انفعالات پاتوفیزیولوژیک در سیستم عصبی مرکزی و محیطی را در بر میگیرد. این اختلال که بیش از یک میلیارد نفر را تحت تأثیر قرار داده است، به ویژه در افرادی که در گروههای با سطح خطر بالا قرار دارند، نیازمند یک رویکرد مدیریت استراتژیک است که بر درک عمیق مکانیسمهای بیولوژیکی و رفتارهای خودمراقبتی استوار باشد. در مرکز این رویکرد، مفهوم “بهداشت میگرن” و “مدیریت آستانه حملات” قرار دارد که هدف آن نه تنها کاهش فراوانی حملات، بلکه افزایش انعطافپذیری سیستم عصبی در برابر محرکهای اجتنابناپذیر است. این گزارش با بررسی مبانی ژنتیکی و کانالوپاتیهای مرتبط با میگرن آغاز شده و سپس به تشریح دقیق ریسکفاکتورهای اصلاحپذیر و ارائه یک پروتکل عملیاتی برای پیشبینی و پیشگیری از حملات میپردازد.
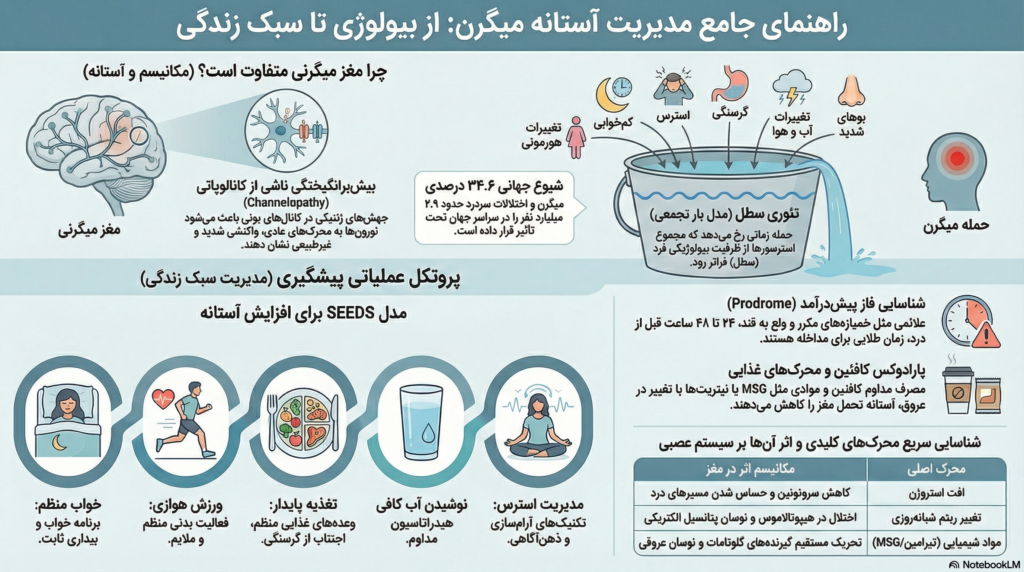
مبانی ژنتیکی و پاتوفیزیولوژی کانالهای یونی: چرا مغز میگرنی متفاوت است؟
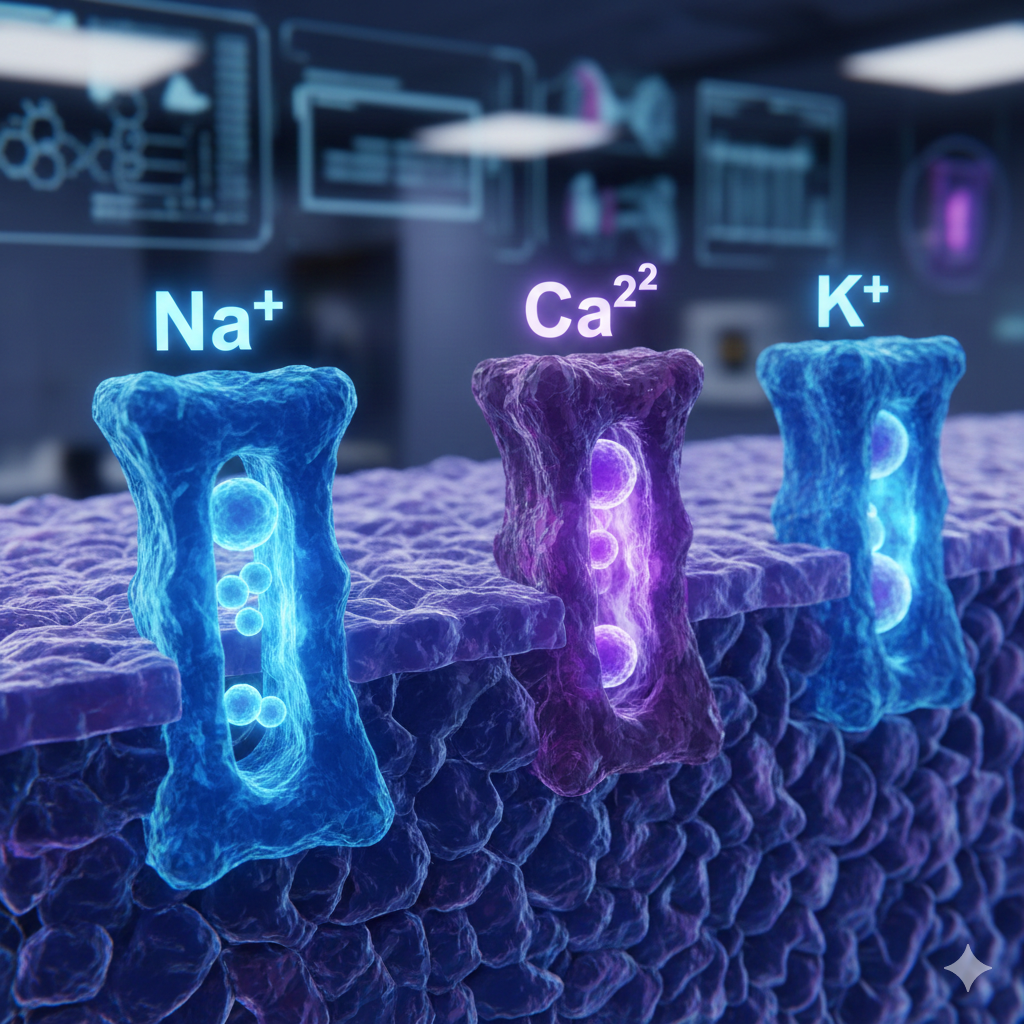
تفاوت بنیادین میان مغز افراد مبتلا به میگرن و افراد غیرمبتلا در سطح “حساسیت” و “واکنشپذیری” نهفته است. تحقیقات نوین در حوزه ژنتیک مولکولی نشان دادهاند که میگرن یک بیماری با زمینه ژنتیکی قوی است که در آن اختلال در عملکرد کانالهای یونی نقش محوری ایفا میکند. کانالهای یونی پروتئینهای غشایی هستند که جریان یونهایی مانند سدیم (Na+)، پتاسیم (K+) و کلسیم (Ca2+) را به داخل و خارج سلولهای عصبی کنترل میکنند و از این طریق پتانسیل غشا و انتقال پیامهای عصبی را تنظیم مینمایند.
مکانیسم کانالوپاتی و بیشبرانگیختگی عصبی
در بسیاری از فرمهای میگرن، به ویژه میگرنهای همیپلژیک فامیلی (FHM)، جهشهای ژنتیکی خاصی منجر به وضعیتی به نام “کانالوپاتی” (Channelopathy) میشود. این اختلالات باعث میشوند که نورونهای مغزی در وضعیتی از “بیشبرانگیختگی” (Hyperexcitability) قرار گیرند، به این معنا که با محرکهایی که برای یک فرد عادی بیاثر هستند، به سرعت دپلاریزه شده و سیگنالهای درد را ارسال میکنند.
چندین ژن کلیدی در این فرآیند شناسایی شدهاند:
- ژن CACNA1A: این ژن مسئول کدگذاری بخشی از کانالهای کلسیم نوع P/Q وابسته به ولتاژ در پایانههای عصبی است. جهشهای “افزایش عملکرد” (Gain-of-function) در این ژن منجر به ورود بیش از حد کلسیم به نورون و در نتیجه آزادسازی مقادیر غیرطبیعی گلوتامات (اصلیترین انتقالدهنده عصبی تحریککننده) در سیناپسها میگردد.
- ژن ATP1A2: این ژن پمپ سدیم-پتاسیم (Na+/K+-ATPase) را در سلولهای آستروسیت کنترل میکند. اختلال در این پمپ باعث تجمع پتاسیم و گلوتامات در فضای خارج سلولی میشود که بازگشت نورون به حالت استراحت را دشوار ساخته و پایداری وضعیت تحریک را تقویت میکند.
- ژن SCN1A: این ژن کانالهای سدیم وابسته به ولتاژ را کدگذاری میکند. جهش در این کانالها باعث تسریع در انتشار پتانسیل عمل و تسهیل وقوع پدیدهای به نام “افسردگی گسترشیافته قشری” (CSD) میشود.
| نام ژن | نوع کانال/پمپ درگیر | پیامد مولکولی | اثر بالینی در میگرن |
|---|---|---|---|
| CACNA1A | کانال کلسیم (Ca_v2.1) | افزایش آزادسازی گلوتامات | تحریکپذیری قشر مغز و ایجاد آورا |
| ATP1A2 | پمپ Na+/K+ | عدم پاکسازی گلوتامات و پتاسیم | کاهش آستانه تحریک و تداوم حملات |
| SCN1A | کانال سدیم (Na_v1.1) | تسریع دپلاریزاسیون سلولی | افزایش سرعت انتقال پیام درد |
| KCNK18 | کانال پتاسیم (TRESK) | نقص در هایپرپلاریزاسیون | ناتوانی نورون در سرکوب تحریکات |
پدیده افسردگی گسترشیافته قشری (CSD)
این حساسیت ژنتیکی زمینهساز پدیده CSD است؛ موجی از فعالیت الکتریکی شدید که به دنبال آن یک دوره خاموشی عصبی در قشر مغز رخ میدهد. CSD نه تنها مسئول ایجاد علائم بینایی و حسی “آورا” است، بلکه باعث فعال شدن پایانه اعصاب تریژمینال (سه قلو) در عروق خونی مغز (سیستم تریژمینواسکولار) میشود. فعال شدن این سیستم منجر به آزاد شدن پپتید مرتبط با ژن کلسیتونین (CGRP) میگردد که یک وازودیلاتور (گشادکننده عروق) قدرتمند و واسطه اصلی التهاب عصبی و درد ضرباندار در میگرن است.
تئوری آستانه میگرن: مدل بار تجمعی و ظرفیت تحمل
برای مدیریت کاربردی میگرن، درک مفهوم “آستانه” (Threshold) ضروری است. تئوری آستانه بیان میکند که حمله میگرن یک رویداد تکعاملی نیست، بلکه نتیجه انباشت چندین استرسور در یک بازه زمانی کوتاه است.
استعاره سطل و آب
این تئوری اغلب با استعاره یک سطل یا فنجان توضیح داده میشود:
- اندازه سطل: نشاندهنده آستانه بیولوژیکی و ژنتیکی فرد است. افرادی که جهشهای کانال یونی دارند، سطل کوچکتری دارند.
- آب داخل سطل: نشاندهنده محرکها (Triggers) است. هر محرک مانند یک قطره یا یک پارچ آب به سطل اضافه میشود.
- سرریز شدن سطل: زمانی که مجموع محرکها از ظرفیت سطل فراتر رود، حمله میگرن آغاز میشود.
یک محرک به تنهایی (مثلاً بوی عطر همکار) ممکن است در یک روز عادی که فرد خواب کافی داشته و استرسی ندارد، باعث حمله نشود. اما اگر همین محرک با کمخوابی، گرسنگی و تغییرات هورمونی همراه شود، سطل سرریز خواهد کرد. بنابراین، مدیریت میگرن شامل دو استراتژی اصلی است: کاهش میزان آب ورودی (مدیریت محرکها) و افزایش عمق سطل (بالا بردن آستانه از طریق بهداشت میگرن).
تحلیل ریسکفاکتورهای اصلاحپذیر: مکانیسمها و راهبردهای مداخله
بیماران با سطح خطر بالا باید بر ریسکفاکتورهایی تمرکز کنند که کنترل آنها در اختیار خودشان است. این عوامل شامل الگوی خواب، نوسانات هورمونی و محرکهای بیوشیمیایی ناشی از تغذیه است.
۱. فیزیولوژی خواب و ریتمهای شبانهروزی
خواب یکی از قدرتمندترین تنظیمکنندههای آستانه میگرن است. مغز میگرنی به شدت به تغییرات در الگوی خواب حساس است.
- کمخوابی و بیشخوابی: هر دو حالت میتوانند محرک باشند. کمخوابی باعث افزایش سطح پروتئینهای التهابی و حساسیت سیستم تریژمینال میشود. از سوی دیگر، خواب بیش از حد در روزهای تعطیل (Let-down headache) به دلیل افت ناگهانی آدرنالین و تغییر در سطح دیاکسید کربن خون، منجر به اتساع عروق و شروع حمله میگردد.
- اختلالات ریتم شبانهروزی: هیپوتالاموس، که ساعت مرکزی بدن است، در افراد میگرنی حساسیت بالایی دارد. تغییر در زمان بیداری، حتی به میزان یک ساعت، میتواند باعث اختلال در آزادسازی ملاتونین و کورتیزول شده و آستانه را پایین بیاورد.
| اقدام پیشنهادی | مکانیسم اثر | هدف درمانی |
|---|---|---|
| زمانبندی ثابت | تثبیت هیپوتالاموس و ریتم شبانهروزی | جلوگیری از نوسان پتانسیل الکتریکی مغز |
| محدودیت ۷-۹ ساعت | تعادل در سطوح آدرنالین و ملاتونین | پیشگیری از سردردهای ناشی از “رها شدن استرس” |
| محیط خنک و تاریک | کاهش تحریک سیستم لیمبیک | افزایش کیفیت خواب عمیق (REM) |
| اجتناب از کافئین قبل خواب | مهار رقابتی گیرندههای آدنوزین | جلوگیری از بیداریهای مکرر شبانه |
۲. نوسانات هورمونی: محور استروژن-سروتونین
در زنان، نوسانات هورمونی یکی از شایعترین محرکهای داخلی است. “تئوری افت استروژن” بیان میکند که کاهش سریع سطح استروژن در اواخر فاز لوتئال (قبل از قاعدگی) محرک اصلی میگرن قاعدگی است.
مکانیسم مولکولی: استروژن بر بیان آنزیمهای متابولیزه کننده سروتونین (مانند MAO) تأثیر میگذارد. افت استروژن باعث کاهش سطح سروتونین میشود که خود منجر به آزادسازی بیرویه CGRP و حساس شدن مسیرهای درد تریژمینال میگردد.
تأثیرات در طول عمر: میگرن اغلب در دوران بلوغ آغاز شده، در دوران بارداری (به دلیل سطوح بالای و ثابت استروژن) بهبود یافته و در دوران یائسگی به دلیل نوسانات شدید هورمونی تشدید میشود.
۳. محرکهای غذایی و ثبات متابولیک
بسیاری از بیماران به اشتباه تصور میکنند که باید لیست بلندی از غذاها را حذف کنند. اما تحقیقات نشان میدهد که “نحوه غذا خوردن” به اندازه “نوع غذا” اهمیت دارد.
- افت قند خون (Hypoglycemia): حذف وعدههای غذایی یا روزهداری باعث نوسان در سطح گلوکز خون میشود. مغز برای عملکرد صحیح به انرژی پایداری نیاز دارد؛ افت قند خون باعث فعال شدن پاسخهای استرسی و آزادسازی گلوتامات میشود که آستانه را به شدت کاهش میدهد.
- مواد بیوشیمیایی محرک:
- تیرامین: این ماده که در پنیرهای کهنه و غذاهای فرآوری شده یافت میشود، به عنوان یک سمپاتومیمتیک عمل کرده و باعث آزادسازی نوراپینفرین و تغییر در قطر عروق خونی میشود.
- نیتریتها و نیتراتها: این مواد که در گوشتهای فرآوری شده (سوسیس، کالباس) وجود دارند، به اکسید نیتریک تبدیل شده و باعث گشادی مستقیم عروق مغزی میشوند.
- MSG: گلوتامات موجود در MSG مستقیماً با گیرندههای NMDA در مغز تعامل داشته و باعث افزایش تحریکپذیری عصبی میگردد.
| ماده شیمیایی | منابع شایع | مکانیسم در میگرن |
|---|---|---|
| تیرامین | پنیرهای کهنه، شراب قرمز، غذاهای تخمیری | آزادسازی نوراپینفرین و نوسان عروقی |
| نیتریتها | ژامبون، بیکن، هاتداگ | افزایش سطوح اکسید نیتریک و وازودیلاتاسیون |
| MSG | غذاهای فرآوری شده، چاشنیها | تحریک مستقیم گیرندههای گلوتامات |
| آسپارتام | نوشابههای رژیمی، آدامسهای بدون قند | اختلال در سنتز انتقالدهندههای عصبی |
۴. کافئین و الکل: پارادوکس درمان و تحریک
کافئین و گیرندههای آدنوزین
کافئین ساختاری مشابه آدنوزین دارد و به گیرندههای A_1 و A_{2A} در مغز متصل میشود.
- اثر درمانی: در دوزهای کوچک (۲۵-۱۰۰ میلیگرم)، کافئین باعث انقباض عروق گشاد شده و جذب داروهای مسکن را تسریع میکند.
- اثر محرک: مصرف مداوم باعث “بیشتنظیمی” (Up-regulation) گیرندههای آدنوزین میشود. هنگامی که سطح کافئین در خون افت میکند (مثلاً صبح زود)، آدنوزین بیش از حد به گیرندههای جدید متصل شده و باعث گشادی شدید عروق و سردرد بازگشتی (Rebound) میگردد.
الکل، هیستامین و کونژنرها
الکل از سه طریق باعث حمله میشود:
- اتانول: مستقیماً باعث گشادی عروق و کمآبی بدن میشود.
- هیستامین: الکل نه تنها حاوی هیستامین است، بلکه آنزیمهای مسئول تجزیه هیستامین در روده را نیز مهار میکند که منجر به پاسخهای التهابی میشود.
- کونژنرها (Congeners): این مواد که در مشروبات الکلی تیره (مانند شراب قرمز و ویسکی) بیشتر یافت میشوند، سموم جانبی تخمیر هستند که باعث استرس اکسیداتیو در سیستم عصبی میشوند.
راهنمای کاربردی گامبهگام برای مدیریت آستانه و پیشبینی حملات
بیمار با سطح خطر بالا باید از یک مدل مدیریتی فعال استفاده کند که شامل مراحل زیر است:
- گام اول: شناسایی و مداخله در فاز پرودروم (Prodrome)
میگرن معمولاً ۲۴ تا ۴۸ ساعت قبل از شروع درد، با علائم هشداردهنده آغاز میشود. شناسایی این علائم به بیمار اجازه میدهد تا قبل از “سرریز شدن سطل” اقدام کند.
علائم کلیدی: خمیازههای مکرر، ولع به مواد قندی، سفتی گردن، حساسیت به نور و تغییرات خلقی (تحریکپذیری یا سرخوشی).
اقدامات اضطراری: مصرف آب و الکترولیتها برای مقابله با کمآبی احتمالی. تمرینات تنفسی عمیق یا بیوفیدبک برای کاهش تنش سیستم سمپاتیک. استفاده از عینکهای تیره یا رفتن به محیطی کمنور برای کاهش بار حسی مغز. - گام دوم: پروتکل دفترچه یادداشت میگرن (Headache Diary)
ردیابی دقیق تنها راه برای کشف الگوهای شخصی است. دفترچه یادداشت باید شامل موارد زیر باشد:
شدت و مکان درد: مقیاس ۰ تا ۱۰ و مشخص کردن یکطرفه یا دوطرفه بودن.
علائم همراه: تهوع، حساسیت به نور/صدا و وجود آورا.
پنجره ۲۴ ساعته محرکها: ثبت دقیق مصرف کافئین، الکل، زمان خواب و وعدههای غذایی قبل از حمله.
چرخه هورمونی: روزهای قاعدگی برای شناسایی میگرنهای مرتبط با هورمون. - گام سوم: استراتژی افزایش آستانه (بهداشت میگرن)
بیمار باید رفتارهای خود را بر اساس مدل SEEDS تنظیم کند که مخفف پنج رکن اصلی سلامت مغز میگرنی است:
S (Sleep): بیداری در ساعت مشخص، حتی در روزهای جمعه.
E (Exercise): ورزش هوازی منظم (مانند ۴۰ دقیقه پیادهروی سریع ۳ بار در هفته) که به اندازه داروهای پیشگیرانه در کاهش حملات مؤثر است.
E (Eating): مصرف وعدههای کوچک و مکرر برای جلوگیری از افت قند خون.
D (Drinking): نوشیدن ۱.۵ تا ۲ لیتر آب در روز.
S (Stress): استفاده از تکنیکهای مدیریت استرس مانند مدیتیشن یا یوگا برای کاهش سطح کورتیزول. - گام چهارم: مدیریت هوشمند محرکهای محیطی
بیماران با خطر بالا باید محیط خود را “میگرنزدایی” کنند:
نورپردازی: استفاده از لامپهای با طیف گرم و اجتناب از نورهای فلورسنت یا چشمکزن.
ارگونومی: اصلاح وضعیت نشستن پشت کامپیوتر برای جلوگیری از فشار به عضلات گردن و تحریک اعصاب گردنی که با عصب تریژمینال ارتباط دارند.
بوهای تند: حذف عطرها، خوشبوکنندههای هوا و شویندههای با بوی تند از محیط خانه و کار.
استفاده از فناوری در پیشبینی حملات: آینده مدیریت میگرن
امروزه ابزارهای پیشرفتهای برای پایش فیزیولوژیک در دسترس هستند که میتوانند به بیمار در پیشبینی حملات کمک کنند.
شاخص تغییرپذیری ضربان قلب (HRV) و فشار بارومتریک
تحقیقات نشان میدهند که کاهش در HRV (نشاندهنده غلبه سیستم عصبی سمپاتیک و استرس) اغلب ۲۴ ساعت قبل از شروع درد رخ میدهد. گجتهای پوشیدنی مانند حلقههای هوشمند یا ساعتهای سلامت میتوانند این تغییرات را رصد کنند.
علاوه بر این، افت فشار بارومتریک (تغییر آب و هوا) باعث تغییر در فشار سینوسها و عروق مغزی میشود. بیمارانی که از این تغییرات آگاه هستند، میتوانند در روزهای پرخطر، استرس خود را کاهش داده و از محرکهای دیگر دوری کنند تا سطلشان سرریز نشود.
| نشانگر زیستی | وضعیت قبل از حمله | معنای فیزیولوژیک |
|---|---|---|
| HRV (تغییرپذیری ضربان قلب) | کاهش معنادار | استرس سیستم عصبی خودمختار |
| دمای پوست | نوسانات غیرطبیعی | اختلال در تنظیم عروق محیطی |
| کارایی خواب | کاهش کیفیت و بیداری مکرر | تحریکپذیری اولیه هیپوتالاموس |
| فشار هوا | افت ناگهانی | تحریک گیرندههای فشار در پردههای مغز |
نتیجهگیری و تحلیل نهایی
مدیریت میگرن در بیماران با سطح خطر بالا، فراتر از مصرف داروهای مسکن است. این فرآیند نیازمند پذیرش این واقعیت است که مغز میگرنی دارای یک ساختار ژنتیکی خاص با کانالهای یونی فوقحساس است که به تغییرات محیطی واکنش نشان میدهد.
استراتژی موفق بر سه پایه استوار است:
- آموزش: درک تئوری آستانه به بیمار کمک میکند تا از خودسرزنشی به دلیل وقوع حملات دست برداشته و بر عوامل قابل کنترل تمرکز کند.
- ثبات: مغز میگرنی تشنه روتین است. ثبات در خواب، تغذیه و هیدراتاسیون، نوسانات الکتریکی مغز را به حداقل میرساند.
- هوشیاری: شناسایی فاز پرودروم و استفاده از ابزارهای ردیابی، قدرت پیشبینی را به بیمار بازمیگرداند و اجازه میدهد مداخلات در زمانی انجام شوند که بیشترین اثربخشی را دارند.
اجرای دقیق پروتکل بهداشت میگرن، اگرچه نیازمند انضباط شخصی بالایی است، اما میتواند منجر به کاهش چشمگیر در تعداد “روزهای از دست رفته” زندگی و جلوگیری از تبدیل میگرن اپیزودیک به میگرن مزمن شود. در نهایت، هدف اصلی این است که بیمار به جای واکنش نشان دادن به درد، با مدیریت هوشمندانه سبک زندگی، بر بیماری خود مسلط شود.
بازبینی توسط متخصص
بازبین علمی این مقاله
آیا میگرن در خانواده شما ارثی است؟
با توجه به نقش کلیدی کانالوپاتیهای ژنتیکی در بروز میگرن، درک زمینه ژنتیکی شما میتواند به تدوین پروتکلهای بهداشت عصبی و دارویی دقیقتر کمک کند. تیم ما آماده ارائه مشاوره ژنتیک تخصصی در این زمینه است.
دریافت مشاوره ژنتیک