آناتومی جراحی و مدیریت بالینی فتقهای اینگوینال
نقشه یادگیری این مقاله
۱. پادکست: برای درک کلی، ابتدا به پادکست گوش دهید.
۲. ویدیو: ویدیو آموزشی را برای یادگیری عمیق مشاهده کنید.
۳. مطالعه متن: در نهایت، متن مقاله را به عنوان منبع جامع مرور کنید.
مشاهده ویدیو در آپارات
گزارش جامع تحقیقاتی: پاتولوژی ساختاری، آناتومی جراحی و مدیریت بالینی فتقهای اینگوینال
تحلیل عمیق مکانیسمهای مولکولی، آناتومیک و استراتژیهای درمانی
۱. مقدمه و اهمیت بالینی
فتق اینگوینال (Inguinal Hernia) به عنوان یکی از شایعترین پاتولوژیهای جراحی در سراسر جهان شناخته میشود که نه تنها بار قابل توجهی بر سیستمهای بهداشتی تحمیل میکند، بلکه در صورت عدم مدیریت صحیح، میتواند منجر به عوارض تهدیدکننده حیات نظیر استرانگولاسیون (Strangulation) و نکروز روده گردد. اگرچه این عارضه اغلب به عنوان یک نقص مکانیکی ساده در دیواره شکم تلقی میشود، اما پاتوفیزیولوژی زیربنایی آن شامل تعامل پیچیده ای از عوامل جنینشناسی، بیولوژی مولکولی بافت همبند، تغییرات بیومکانیکی و فشارهای هیدرواستاتیک داخل شکمی است. درک عمیق از آناتومی کانال اینگوینال و مکانیسمهای شکست دیواره شکم، برای تمایز بین انواع مختلف فتق و تعیین فوریتهای جراحی امری حیاتی است. این گزارش با رویکردی جامع، به تشریح دقیق آناتومی، پاتولوژی ساختاری، و تمایزات بالینی حیاتی در فتقهای اینگوینال میپردازد و بر اساس شواهد موجود، فوریتهای مداخله در موارد استرانگوله را تبیین میکند.
۲. جنینشناسی و تکامل کانال اینگوینال
درک پاتولوژی فتقهای اینگوینال، به ویژه نوع غیرمستقیم (Indirect)، بدون شناخت دقیق وقایع جنینشناسی امکانپذیر نیست. کانال اینگوینال در واقع مسیری است که در طی تکامل جنینی برای نزول گنادها (بیضهها در مردان و تخمدانها/لیگامان گرد در زنان) ایجاد میشود.
۲.۱ نزول بیضه و نقش گوبرناکولوم
در طی دوره جنینی، بیضهها در دیواره خلفی شکم و در ناحیه رتروپریتونئال شکل میگیرند. نزول آنها به داخل کیسه بیضه (اسکروتوم) توسط ساختاری طنابمانند به نام گوبرناکولوم (Gubernaculum) هدایت میشود. این ساختار مزانشیمی، قطب تحتانی گناد را به چینهای لبیواسکروتال (که بعداً اسکروتوم یا لابیا ماژور را تشکیل میدهند) متصل میکند. گوبرناکولوم با ایجاد مسیری در میان لایههای عضلانی دیواره قدامی شکم، کانال اینگوینال را شکل میدهد.
۲.۲ زائده واژینال (Processus Vaginalis)
همزمان با نزول بیضه، یک برآمدگی کیسهمانند از صفاق (پریتونئوم) به نام زائده واژینال (Processus Vaginalis) همراه با بیضه و در جلوی طناب اسپرماتیک وارد کانال اینگوینال میشود. این زائده صفاقی در واقع امتداد مستقیم حفره شکمی به داخل اسکروتوم است. در یک روند فیزیولوژیک طبیعی، پس از نزول کامل بیضه، لایههای پروگزیمال زائده واژینال باید دچار تحلیل (Obliteration) شوند و بسته گردند. بخش دیستال این زائده در اطراف بیضه باقی میماند و تونیکا واژینالیس (Tunica Vaginalis) را تشکیل میدهد که اجازه تحرک بیضه در اسکروتوم را میدهد. شکست در این پروسه بسته شدن، زیربنای اصلی فتقهای اینگوینال مادرزادی (غیرمستقیم) است که در بخشهای بعدی به تفصیل بحث خواهد شد.
۳. آناتومی جراحی دقیق ناحیه اینگوینال
آناتومی ناحیه اینگوینال به دلیل لایههای متعدد فاسیا و عضله و درهمآمیختگی آنها پیچیده است. شناخت دقیق این لایهها برای درک مکانیسمهای شکست دیواره شکم ضروری است.
۳.۱ منفذ مایوپکتینئال فروشو (Myopectineal Orifice of Fruchaud)
در جراحی مدرن فتق، مفهوم کانال اینگوینال جای خود را به مفهوم جامعتر منفذ مایوپکتینئال (MPO) داده است که توسط هنری فروشو (Henri Fruchaud) در سال ۱۹۵۶ توصیف شد. این منفذ یک ناحیه ضعف ذاتی در دیواره تحتانی شکم است که تمامی انواع فتقهای کشاله ران (اینگوینال مستقیم، غیرمستقیم و فمورال) از طریق آن رخ میدهند.
مرزهای دقیق منفذ مایوپکتینئال عبارتند از:
- فوقانی: الیاف قوسیشکل (Arching fibers) عضلات مایل داخلی (Internal Oblique) و عرضی شکم (Transversus Abdominis).
- تحتانی: راموس فوقانی استخوان پوبیس که توسط لیگامان پکتینئال (لیگامان کوپر) پوشیده شده است.
- داخلی (مدیال): عضله راست شکمی (Rectus Abdominis) و غلاف آن.
- خارجی (لترال): عضله ایلیوپسواس (Iliopsoas).
لیگامان اینگوینال (لیگامان پوپار) از میان این منفذ عبور کرده و آن را به دو ناحیه تقسیم میکند: ناحیه فوقانی که محل عبور طناب اسپرماتیک و بروز فتقهای اینگوینال است، و ناحیه تحتانی که محل عبور عروق فمورال و بروز فتقهای فمورال میباشد. اهمیت بالینی این مفهوم در جراحیهای لاپاراسکوپیک و ترمیم با مش است، جایی که هدف پوشش کامل این منفذ برای پیشگیری از هر نوع فتق کشاله ران است.
۳.۲ کانال اینگوینال: دیوارهها و ساختار
کانال اینگوینال یک تونل مورب به طول تقریبی ۴ تا ۶ سانتیمتر در بزرگسالان است که موازی و در بالای نیمه داخلی لیگامان اینگوینال قرار دارد. دیوارههای این کانال با استفاده از واژهیار “2MALT” (۲ عضله، ۲ آپونوروز، ۲ لیگامان، ۲ تاندون) قابل یادآوری هستند.
۳.۲.۱ دیواره قدامی (Anterior Wall)
این دیواره عمدتاً توسط آپونوروز عضله مایل خارجی (External Oblique Aponeurosis) تشکیل شده است. در بخشهای لترال (خارجی)، الیاف گوشتی عضله مایل داخلی نیز به تقویت این دیواره کمک میکنند. نقص در این آپونوروز در ناحیه مدیال، حلقه سطحی اینگوینال (Superficial Inguinal Ring) را میسازد که محل خروج طناب اسپرماتیک از کانال است.
۳.۲.۲ دیواره خلفی یا کف آناتومیک (Posterior Wall)
دیواره خلفی حیاتیترین ساختار در پاتولوژی فتقهای مستقیم است. این دیواره عمدتاً توسط فاسیای ترانسورسالی (Transversalis Fascia) تشکیل شده است. فاسیای ترانسورسالی لایهای نازک اما مهم است که حفره شکمی را محصور میکند. در ناحیه مدیال، ادغام آپونوروز عضلات مایل داخلی و عرضی شکم، ساختاری محکم به نام تاندون مشترک (Conjoint Tendon) یا داس اینگوینال (Falx Inguinalis) را ایجاد میکند که دیواره خلفی را تقویت میکند. ضعف در این دیواره، به ویژه در مثلث هسلباخ، منجر به فتق مستقیم میشود.
۳.۲.۳ سقف (Roof)
سقف کانال توسط الیاف قوسیشکل عضلات مایل داخلی (Internal Oblique) و عرضی شکم (Transversus Abdominis) تشکیل میشود. این الیاف از روی طناب اسپرماتیک عبور کرده و به سمت مدیال قوس میزنند تا به تاندون مشترک تبدیل شوند. انقباض این عضلات نقش مهمی در مکانیسم دفاعی فیزیولوژیک کانال (مکانیسم شاتر) دارد.
۳.۲.۴ کف (Floor)
کف کانال توسط لیگامان اینگوینال (Inguinal Ligament) شکل میگیرد که خود حاصل برگشتن لبه تحتانی آپونوروز مایل خارجی به سمت داخل است. در سمت مدیال، لیگامان لاکونار (Lacunar Ligament) نیز در تشکیل کف مشارکت دارد.
| مرز (Boundary) | ساختارهای تشکیلدهنده | اهمیت بالینی |
|---|---|---|
| دیواره قدامی | آپونوروز مایل خارجی | محل قرارگیری حلقه سطحی؛ سد اولیه در برابر بیرونزدگی قدامی |
| دیواره خلفی | فاسیای ترانسورسالی و تاندون مشترک | ناحیه ضعف در فتقهای مستقیم؛ شکست در این لایه پاتولوژی اصلی است |
| سقف | الیاف قوسی عضلات مایل داخلی و عرضی | مسئول مکانیسم شاتر؛ آتروفی این عضلات باعث باز ماندن کانال میشود |
| کف | لیگامان اینگوینال و لیگامان لاکونار | لبه تحتانی کانال؛ لیگامان لاکونار مرز داخلی کانال فمورال است |
۳.۳ مثلث هسلباخ (Hesselbach’s Triangle)
برای درک پاتولوژی فتق مستقیم، شناخت مثلث اینگوینال یا مثلث هسلباخ ضروری است. این مثلث ناحیهای در دیواره خلفی کانال اینگوینال است که فاقد پوشش عضلانی کامل بوده و تنها توسط فاسیای ترانسورسالی پوشیده شده است.
مرزهای مثلث هسلباخ عبارتند از:
- مدیال (داخلی): لبه خارجی عضله رکتوس شکمی (Rectus Abdominis).
- لترال (خارجی): عروق اپیگاستریک تحتانی (Inferior Epigastric Vessels).
- تحتانی: لیگامان اینگوینال.
فتقهایی که از داخل این مثلث بیرون میزنند، فتق مستقیم نامیده میشوند زیرا مستقیماً از دیواره خلفی عبور میکنند، در حالی که فتقهای غیرمستقیم از حلقه عمقی (که در لترال عروق اپیگاستریک قرار دارد) وارد کانال میشوند.
۴. پاتولوژی ساختاری و مکانیسمهای شکست
توسعه فتق اینگوینال نتیجه شکست تعادل بین فشار داخل شکمی (IAP) و مقاومت دیواره شکم است. این شکست میتواند ناشی از یک نقص مادرزادی آناتومیک و یا ضعف اکتسابی بافتی باشد.
۴.۱ مکانیسمهای مادرزادی: شکست در بسته شدن زائده واژینال (Patent Processus Vaginalis)
پاتولوژی اصلی در فتقهای اینگوینال غیرمستقیم (Indirect)، وجود یک کانال صفاقی باز یا Patent Processus Vaginalis (PPV) است.
مکانیسم: اگر زائده واژینال پس از نزول بیضه بسته نشود، مسیری مستقیم بین حفره صفاقی و اسکروتوم باقی میماند. افزایش فشار داخل شکمی (گریه کردن در نوزادان، زور زدن) باعث رانده شدن محتویات شکم (روده باریک یا امنتوم) به داخل این ساک باز میشود.
شیوع: مطالعات نشان میدهند که PPV بدون علامت در درصد قابل توجهی از بزرگسالان نیز وجود دارد (تا ۲۲٪ در افراد زیر ۲۰ سال و ۱۴٪ در افراد بالای ۵۰ سال). این یافته بیانگر آن است که اگرچه PPV شرط لازم برای فتق غیرمستقیم است، اما شرط کافی نیست و عوامل دیگری مانند فشار مزمن احتمالاً برای باز کردن بالینی فتق در بزرگسالان نقش دارند.
مسیر آناتومیک: ساک فتق از طریق حلقه عمقی اینگوینال (Deep Ring) که در لترال عروق اپیگاستریک قرار دارد، وارد کانال میشود و درون طناب اسپرماتیک به سمت پایین حرکت میکند.
۴.۲ مکانیسمهای اکتسابی: ضعف بافت همبند و فاسیای ترانسورسالی
فتقهای مستقیم (Direct) معمولاً اکتسابی هستند و ناشی از ضعف پیشرونده در دیواره خلفی کانال (فاسیای ترانسورسالی) در ناحیه مثلث هسلباخ میباشند.
۴.۲.۱ بیولوژی کلاژن و متالوپروتئینازهای ماتریکس (MMPs)
تحقیقات مدرن نشان دادهاند که فتق اینگوینال تنها یک نقص مکانیکی نیست، بلکه تظاهری از یک بیماری سیستمیک بافت همبند است.
- نسبت کلاژن: استحکام دیواره شکم به کلاژن نوع I (که فیبرهای ضخیم و با استحکام کششی بالا میسازد) وابسته است. در بیماران مبتلا به فتق اینگوینال، کاهشی معنادار در نسبت کلاژن نوع I به کلاژن نوع III مشاهده شده است. کلاژن نوع III نازکتر و نابالغتر است و استحکام مکانیکی کمتری دارد.
- نقش آنزیمها: افزایش فعالیت آنزیمهای تجزیهکننده کلاژن مانند MMP-2 و تغییر در تعادل MMP-1 و MMP-13 در فیبروبلاستهای فاسیای ترانسورسالی بیماران فتق مشاهده شده است. عواملی مانند سیگار کشیدن با القای فعالیت پروتئازها و مهار سنتز کلاژن، این روند تخریبی را تشدید کرده و خطر فتقهای اکتسابی و عود آنها را افزایش میدهند.
۴.۳ نارسایی بیومکانیکی: شکست مکانیسم شاتر (Shutter Mechanism)
کانال اینگوینال دارای مکانیسمهای دفاعی فیزیولوژیک است که در زمان افزایش فشار داخل شکم (مانند سرفه)، کانال را میبندند.
عملکرد طبیعی: در هنگام انقباض عضلات شکم، الیاف قوسی عضله مایل داخلی و عرضی شکم (سقف کانال) مسطح شده و به سمت پایین (به سمت لیگامان اینگوینال) حرکت میکنند. این حرکت مانند یک دریچه یا شاتر (Shutter) عمل کرده و دیواره خلفی و حلقه عمقی را تقویت و مسدود میکند.
پاتولوژی شکست: در افراد مبتلا به فتق، ممکن است اتصال این عضلات بالاتر از حد معمول باشد یا به دلیل آتروفی، قوس عضلانی نتواند به اندازه کافی پایین بیاید تا کانال را بپوشاند. این نارسایی باعث میشود دیواره خلفی (فاسیای ترانسورسالی) در برابر فشار شکم بیدفاع بماند و به مرور زمان دچار بیرونزدگی (فتق مستقیم) شود.
۴.۴ اتروفی عضلانی نوروپاتیک (Neuropathic Muscle Atrophy)
آسیب به اعصاب ناحیه اینگوینال میتواند منجر به فلج موضعی عضلات محافظتکننده کانال شود.
- نقش عصب ایلیواینگوینال: این عصب به عضلات مایل داخلی و عرضی شکم عصبدهی حرکتی میکند. آسیب یاتروژنیک به این عصب (مثلاً در جراحیهای قبلی آپاندکتومی یا برشهای پایین شکم) میتواند باعث آتروفی بخش پایینی این عضلات شود.
- نتیجه: از دست رفتن تون عضلانی و فلج مکانیسم شاتر، دیواره خلفی را مستعد فتق مستقیم میکند.
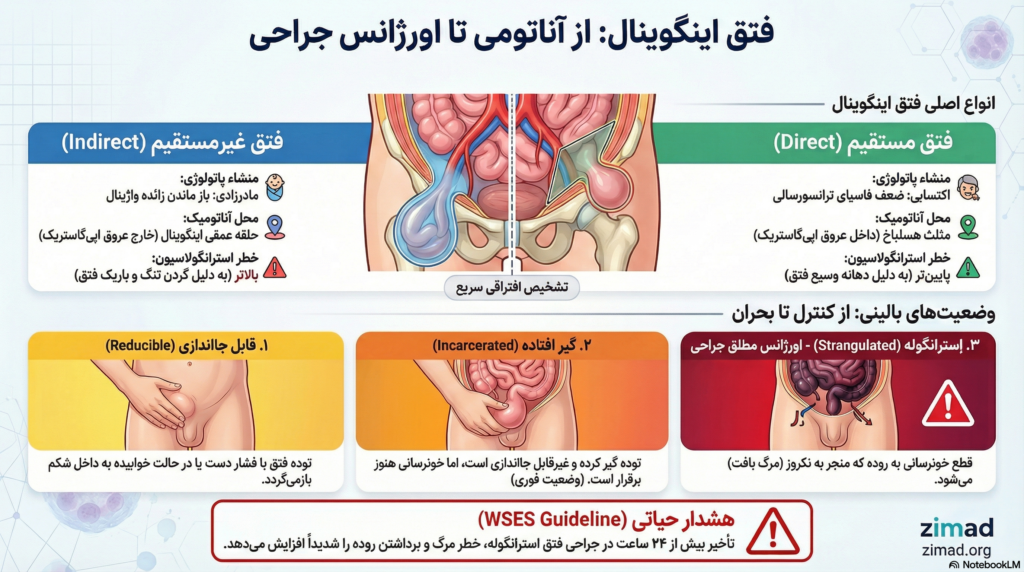
| ویژگی | فتق اینگوینال غیرمستقیم (Indirect) | فتق اینگوینال مستقیم (Direct) |
|---|---|---|
| منشاء آناتومیک | حلقه عمقی اینگوینال (لترال به عروق اپیگاستریک) | مثلث هسلباخ (مدیال به عروق اپیگاستریک) |
| پاتولوژی اولیه | مادرزادی (باز ماندن زائده واژینال) | اکتسابی (ضعف فاسیای ترانسورسالی و کلاژن) |
| مکانیسم عبور | داخل طناب اسپرماتیک حرکت میکند؛ اغلب وارد اسکروتوم میشود | پشت طناب اسپرماتیک برآمده میشود؛ به ندرت وارد اسکروتوم میشود |
| گروه سنی | شایعتر در کودکان و جوانان | شایعتر در سالمندان (به دلیل تحلیل بافتی) |
| خطر استرانگولاسیون | بالاتر (حلقه عمقی باریک است) | پایینتر (مثلث هسلباخ دهانه وسیعتری دارد) |
۵. تمایز بالینی و پاتوفیزیولوژی عوارض: قابل جااندازی، گیر افتاده و استرانگوله
وضعیت بالینی فتق مهمترین فاکتور در تعیین استراتژی درمانی است. فتقها بر اساس قابلیت بازگشت محتویات و وضعیت خونرسانی به سه دسته تقسیم میشوند.
۵.۱ فتقهای قابل جااندازی (Reducible)
در این حالت، محتویات ساک فتق (روده یا امنتوم) را میتوان با دستکاری ملایم یا در حالت استراحت و خوابیدن به داخل حفره شکم بازگرداند.
- علائم: توده نرم در کشاله ران که با سرفه یا ایستادن برجسته میشود و با خوابیدن ناپدید میگردد. درد معمولاً خفیف یا به صورت احساس سنگینی است.
- پاتولوژی: خونرسانی احشاء کاملاً طبیعی است و هیچ انسدادی وجود ندارد.
۵.۲ فتقهای گیر افتاده (Incarcerated)
فتق اینکارسره یا گیر افتاده زمانی رخ میدهد که محتویات فتق در داخل ساک حبس شده و قابلیت جااندازی به حفره شکم را از دست میدهند.
- مکانیسم: چسبندگیهای داخل ساک یا تنگی گردن فتق (در حلقه عمقی یا فمورال) باعث گیر کردن احشاء میشود. ادم ناشی از فشار باعث افزایش حجم محتویات شده و بازگشت آنها را غیرممکن میسازد.
- علائم: توده سفت، دردناک و غیرقابل جااندازی. ممکن است علائم انسداد روده (تهوع، استفراغ، اتساع شکم) وجود داشته باشد اما خونرسانی هنوز به طور کامل قطع نشده است.
- اهمیت: اینکارسراسیون مرحله پیشدرآمد استرانگولاسیون است و باید به عنوان یک وضعیت فوری (Urgent) درمان شود تا از پیشرفت به سمت نکروز جلوگیری گردد.
۵.۳ فتقهای استرانگوله (Strangulated): یک فوریت جراحی
استرانگولاسیون خطرناکترین عارضه فتق است که در آن خونرسانی به احشای گیر افتاده قطع میشود. این یک وضعیت تهدیدکننده حیات است.
پاتوفیزیولوژی ایسکمی:
- انسداد وریدی: فشار وارده از گردن فتق ابتدا وریدهای جدار روده را مسدود میکند. این امر منجر به احتقان شدید، ادم و خونریزی داخل بافتی میشود.
- افزایش فشار بافتی: با افزایش ادم، فشار داخل بافتی از فشار شریانی فراتر رفته و خونرسانی شریانی قطع میشود.
- نکروز و گانگرن: قطع جریان خون شریانی منجر به ایسکمی ترانسمورال، مرگ سلولی و گانگرن روده میشود.
- پرفوراسیون و سپسیس: دیواره نکروزه روده پاره شده و باعث ورود باکتریها و محتویات روده به حفره شکم (پریتونیت) و سپسیس سیستمیک میشود.
علائم بالینی تمایزدهنده:
- درد: درد شدید، مداوم و پیشرونده که حتی در فواصل بین دردهای کولیکی انسداد روده نیز قطع نمیشود.
- علائم موضعی: قرمزی (اریتم)، گرمی و ادم پوست روی توده فتق. توده بسیار حساس به لمس است.
- علائم سیستمیک: تب، تاکیکاردی (ضربان قلب بالا)، لکوسیتوز (افزایش گلبولهای سفید) و علائم شوک سپتیک.
۶. تشخیص و تصویربرداری
تشخیص فتق معمولاً بالینی است، اما در موارد مشکوک یا عوارض پیچیده، تصویربرداری ضروری است.
۶.۱ معاینه فیزیکی
لمس کانال اینگوینال و بررسی وجود توده و “ایمپالس سرفه” (برخورد توده به انگشت هنگام سرفه) اساس تشخیص است. با این حال، تستهای بالینی برای افتراق دقیق فتق مستقیم از غیرمستقیم (مانند انسداد حلقه عمقی با انگشت) همیشه قابل اعتماد نیستند.
۶.۲ نقش سیتیاسکن (CT Scan)
سیتیاسکن استاندارد طلایی تصویربرداری در موارد فتقهای استرانگوله یا اینکارسره است. این روش دارای حساسیت ۹۴-۱۰۰٪ برای تشخیص انسداد و استرانگولاسیون است.
یافتههای سیتیاسکن در استرانگولاسیون:
- ضخیم شدن دیواره روده: ناشی از ادم و ایسکمی.
- علامت هدف (Target Sign): حلقههای متحدالمرکز ادماتوز.
- عدم تقویت (Enhancement): عدم جذب ماده حاجب در دیواره روده نشاندهنده قطع خونرسانی است.
- رشتهرشته شدن چربی (Fat Stranding): التهاب در مزانتر اطراف فتق.
- مایع در ساک: وجود مایع آزاد درون ساک فتق نشانهای با ویژگی (Specificity) بالا برای استرانگولاسیون است.
- پنوماتوزیس (Pneumatosis): وجود گاز در دیواره روده که نشانه نکروز پیشرفته است.
- بیومارکرها: افزایش سطح لاکتات (Lactate)، CPK و D-dimer در خون میتواند پیشبینیکننده ایسکمی روده و استرانگولاسیون باشد.
۷. دستورالعملهای مدیریتی و فوریتهای جراحی (WSES)
بر اساس دستورالعملهای انجمن جهانی جراحی اورژانس (WSES)، مدیریت فتقهای اینگوینال بستگی مستقیم به وضعیت بالینی آنها دارد.
۷.۱ فوریت مداخله
- فتق استرانگوله: بیماران با شک به استرانگولاسیون باید بلافاصله تحت جراحی اورژانسی قرار گیرند (توصیه درجه 1C). تأخیر در جراحی بیش از ۲۴ ساعت به طور چشمگیری خطر رزکسیون روده (برداشتن روده) و مرگومیر را افزایش میدهد.
- فتق فمورال: به دلیل حلقه فمورال تنگ و سخت، فتقهای فمورال دارای خطر بسیار بالای استرانگولاسیون هستند (۲۲٪ در عرض ۳ ماه). بنابراین، تشخیص فتق فمورال به خودی خود اندیکاسیونی برای جراحی فوری یا زودهنگام است، حتی اگر علائم خفیف باشد.
۷.۲ جااندازی دستی (Taxis)
در موارد فتق اینکارسره که علائم قطعی استرانگولاسیون (مانند پریتونیت، اریتم پوستی، لکوسیتوز یا اسیدوز لاکتیک) وجود ندارد، میتوان تلاش برای جااندازی دستی با استفاده از آرامبخش انجام داد. این روش باید “آرام، آماده و ایمن” (GPS Taxis) باشد. در صورت موفقیت، جراحی میتواند به صورت نیمهالکتیو انجام شود؛ اما در صورت شکست، جراحی اورژانسی الزامی است.
۷.۳ تکنیکهای جراحی در موارد اورژانس
- لاپاراسکوپی: در دستان جراح با تجربه، لاپاراسکوپی روشی ایمن برای فتقهای اینکارسره است و امکان ارزیابی زندهبودن روده را بدون برش بزرگ فراهم میکند.
- استفاده از مش: در محیطهای آلوده (مانند زمانی که روده نکروزه برداشته میشود)، استفاده از مشهای مصنوعی دائمی خطر عفونت را افزایش میدهد. در چنین مواردی (زخمهای آلوده یا کثیف)، دستورالعملها پیشنهاد میکنند از ترمیم بافتی اولیه (بدون مش) یا در صورت لزوم از مشهای بیولوژیک استفاده شود. با این حال، در موارد اینکارسره بدون نکروز روده (Clean Field)، استفاده از مش مصنوعی استاندارد (مانند پلیپروپیلن) توصیه میشود (توصیه درجه 1A).
۸. نتیجهگیری
فتق اینگوینال حاصل تلاقی عوامل آناتومیک، جنینی و بیومکانیکی است. فتقهای غیرمستقیم عمدتاً نتیجه باز ماندن مادرزادی زائده واژینال هستند که مسیری مستقیم به داخل کانال ایجاد میکند، در حالی که فتقهای مستقیم ناشی از فرسودگی اکتسابی بافت همبند، اختلال در کلاژنسازی و نارسایی مکانیسم شاتر عضلانی در ناحیه مثلث هسلباخ میباشند. درک دقیق آناتومی منفذ مایوپکتینئال فروشو و لایههای کانال اینگوینال برای جراحی موفق ضروری است.
از منظر بالینی، تمایز حیاتی بین فتقهای قابل جااندازی، اینکارسره و استرانگوله تعیینکننده مرگ و زندگی است. استرانگولاسیون یک فاجعه عروقی است که با ایسکمی و نکروز روده همراه بوده و نیازمند مداخله جراحی فوری است. دستورالعملهای WSES تأکید میکنند که هرگونه تأخیر در مدیریت فتقهای مشکوک به استرانگولاسیون یا فتقهای فمورال غیرقابل پذیرش است، زیرا خطر عوارض و مرگومیر با گذشت زمان به صورت تصاعدی افزایش مییابد.
بازبینی توسط متخصص
بازبین علمی این مقاله
آیا سابقه فتق در خانواده دارید؟
ضعف بافت همبند و اختلال در کلاژنسازی میتواند ریشه ژنتیکی داشته باشد. اگر سابقه فتقهای متعدد یا بیماریهای بافت همبند در خانواده دارید، مشاوره ژنتیک میتواند به درک بهتر ریسک کمک کند.
دریافت مشاوره ژنتیک