گزارش جامع تحقیقاتی: تحلیل پاتوفیزیولوژیک، دینامیک بالینی و اتیولوژی مولکولی زخمهای اثنیعشر (Duodenal Ulcer)
واکاوی عمیق مکانیسمها، عوارض و تمایزات بالینی
مقدمه و چشمانداز کلی
بیماری زخم پپتیک (Peptic Ulcer Disease – PUD) به عنوان یکی از شایعترین پاتولوژیهای دستگاه گوارش فوقانی، نشاندهنده گسستگی در تمام ضخامت مخاطی است که تا زیر مخاط (Submucosa) یا عضلات (Muscularis propria) نفوذ میکند. اگرچه زخمهای معده (Gastric Ulcer – GU) و زخمهای اثنیعشر (Duodenal Ulcer – DU) اغلب تحت یک چتر تشخیصی واحد قرار میگیرند، اما شواهد متراکم فیزیولوژیک و مولکولی نشان میدهد که این دو نهاد بالینی از نظر بیولوژیِ ترشحی، الگوی گاستریت زمینهای، پاسخ به غذا و مکانیسمهای دفاعی مخاطی، تفاوتهای بنیادین و گاهاً متضادی دارند. زخم اثنیعشر که به طور غالب در ناحیه حباب یا پیاز (Bulb) دوازدهه رخ میدهد، نماد کلاسیک وضعیت «هایپرکلرهیدری» (افزایش ترشح اسید) است، در حالی که زخمهای معده اغلب با ترشح نرمال یا کاهشیافته اسید همراه هستند.
درک مدرن ما از پاتوفیزیولوژی DU از مدلهای مکانیکی قرن بیستم عبور کرده و به یک مدل پیچیده ایمونو-میکروبیولوژیک رسیده است. در این مدل، تعامل دینامیک میان عفونت Helicobacter pylori، تغییرات ژنتیکی باکتری (مانند بیان فاز متغیر ادهزینهای SabA و BabA)، اختلال در محور تنظیمکننده نوروهورمونی (محور سوماتواستاتین-گاسترین) و ناتوانی در مکانیسمهای بافری مخاط دوازدهه (مانند متاپلازی معده) نقشهای اصلی را ایفا میکنند. علاوه بر این، شناخت دقیق آناتومی عروقی (بهویژه شریان گاسترودوodenal) و آناتومی فضاهای صفاقی (مانند ناودان پاراکولیک راست) برای درک عوارض حیاتی نظیر خونریزیهای عظیم و سندرمهای نادر پرفوراسیون مانند سندرم والنتینو (Valentino’s Syndrome) ضروری است.
این گزارش با رویکردی exhaustive (جامع و مانع) و با استناد به دادههای دقیق پژوهشی، به تشریح لایههای متعدد پاتوفیزیولوژی، تظاهرات بالینی و عوارض زخمهای اثنیعشر میپردازد.
فصل اول: آناتومی عملکردی و فیزیولوژی ترشح اسید در محور معده-اثنیعشر
برای درک عمیق پاتوفیزیولوژی DU، ابتدا باید زیرساختهای آناتومیک و فیزیولوژیک تنظیمکننده محیط شیمیایی معده و دوازدهه را کالبدشکافی کرد.
۱.۱. میکرواستراکچر و سلولهای تنظیمکننده
مخاط معده از نظر عملکردی به دو واحد متمایز تقسیم میشود که تعامل آنها تعیینکننده خروجی نهایی اسید است:
- مخاط اکسینتیک (Oxyntic Mucosa): این مخاط که بدنه (Corpus) و فوندوس معده را میپوشاند، حاوی سلولهای پاریتال (Parietal Cells) است. این سلولها مجهز به پمپ H+/K+ ATPase هستند که مسئول پمپاژ پروتون به داخل لومن معده است. همچنین سلولهای انتروکروماتینلایک (ECL) در این ناحیه قرار دارند که منبع اصلی هیستامین میباشند.
- مخاط آنترال (Antral Mucosa): ناحیه دیستال معده که فاقد سلولهای پاریتال است اما مرکز فرماندهی هورمونی محسوب میشود. این ناحیه حاوی سلولهای G (ترشحکننده گاسترین) و سلولهای D (ترشحکننده سوماتواستاتین) است.
۱.۲. دینامیک تنظیم ترشح اسید: مکانیزم ترمز و گاز
ترشح اسید تحت کنترل دقیق سه پیامرسان اصلی است:
- هیستامین: قویترین تحریککننده ترشح اسید از طریق گیرندههای H2.
- گاسترین: هورمون پپتیدی که از سلولهای G آنتروم ترشح میشود و سلولهای پاریتال و ECL را تحریک میکند.
- استیلکولین: از عصب واگ آزاد شده و ترشح اسید را تحریک میکند.
مکانیسم فیدبک منفی (The Brake Mechanism): در شرایط فیزیولوژیک سالم، هنگامی که pH آنتروم به کمتر از ۳ میرسد، سلولهای D فعال شده و سوماتواستاتین ترشح میکنند. سوماتواستاتین ترشح گاسترین را متوقف میکند. این مکانیسم حیاتیترین سد در برابر ترشح بیش از حد اسید است که در زخم اثنیعشر دچار نقص میشود.
۱.۳. نقش اسفنکتر پیلور در همودینامیک گوارشی
اسفنکتر پیلور جریان کیموس اسیدی به دوازدهه را کنترل میکند. اختلال در عملکرد پیلور، چه به صورت تخلیه سریع (که بار اسیدی دوازدهه را افزایش میدهد) و چه به صورت رفلاکس صفراوی، در پاتوفیزیولوژی زخمها نقش دارد.
فصل دوم: پاتوفیزیولوژی مولکولی و سلولی زخم اثنیعشر
در اکثریت قاطع موارد DU، عامل محرک اولیه یک عفونت باکتریایی است که فیزیولوژی میزبان را تغییر میدهد.
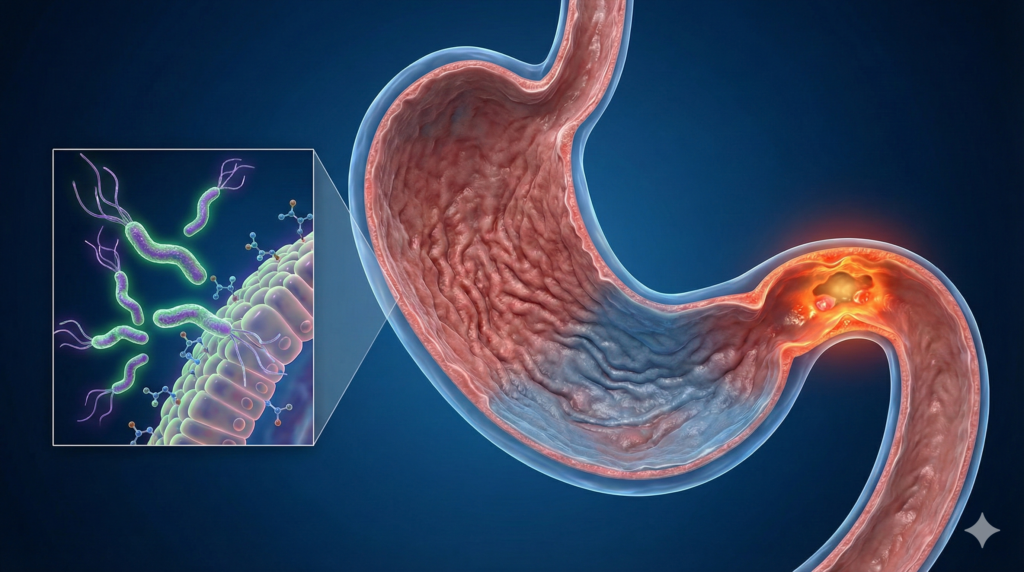
۲.۱. عفونت Helicobacter pylori: فراتر از یک حضور ساده
الگوی توزیع H. pylori در معده تعیینکننده نهایی نوع بیماری است.
۲.۱.۱. الگوی گاستریت آنترال (Antral-Predominant Gastritis)
در بیماران مستعد زخم اثنیعشر، عفونت H. pylori به طور انتخابی در ناحیه آنتروم معده متمرکز میشود، در حالی که بدنه معده (Corpus) سالم باقی میماند. این الگو کلید درک هایپرکلرهیدری در DU است، زیرا سلولهای پاریتال در بدنه سالم باقی مانده و توانایی ترشح اسید را حفظ میکنند.
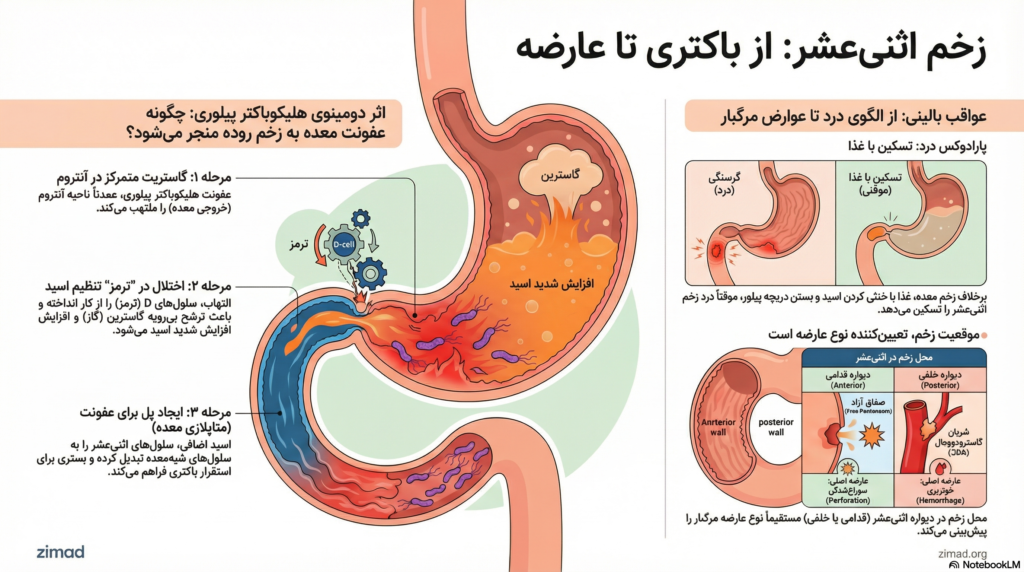
۲.۱.۲. سرکوب سلولهای D و طوفان گاسترین
مکانیسم اصلی افزایش اسید، اختلال در محور سوماتواستاتین-گاسترین است:
- التهاب موضعی: کلونیزاسیون باکتری باعث آزاد شدن سایتوکاینهای التهابی میشود.
- تخریب عملکردی سلولهای D: این واسطهها عملکرد سلولهای D را مختل کرده و ترشح سوماتواستاتین را کاهش میدهند.
- هایپرگاسترینمی: با حذف اثر مهاری سوماتواستاتین (“ترمز”)، سلولهای G گاسترین بیشتری ترشح میکنند.
- هایپرپلازی سلولهای پاریتال: گاسترین باعث افزایش تعداد و حجم سلولهای پاریتال میشود، که منجر به افزایش ظرفیت ترشح اسید میگردد.
۲.۲. متاپلازی معده (Gastric Metaplasia): پل ارتباطی عفونت معده و زخم روده
H. pylori نمیتواند مستقیماً روی اپیتلیوم روده کلونیزه شود. پس چگونه باعث زخم دوازدهه میشود؟
پاسخ در متاپلازی معده است. بار اسیدی بالای معده، مخاط دوازدهه را میسوزاند. در پاسخ، سلولهای دوازدهه به سلولهای نوع معده تبدیل میشوند (متاپلازی) تا مقاومتر شوند. این جزایر متاپلاستیک اکنون بستری برای کلونیزاسیون H. pylori فراهم میکنند که منجر به دوودنیت (التهاب دوازدهه) و زخم میشود.
۲.۳. مکانیسمهای چسبندگی مولکولی: نقش BabA و SabA
پروتئینهای غشای خارجی باکتری نقش کلیدی دارند:
- BabA: به آنتیژنهای گروه خونی Lewis b در سلولهای سالم متصل میشود (استقرار اولیه).
- SabA: به آنتیژنهای التهابی sialyl-Lewis x متصل میشود. این مکانیسم به باکتری اجازه میدهد در بافت ملتهب محکمتر متصل شده و التهاب را تشدید کند.
فصل سوم: دینامیک ترشح اسید و پدیده “فرار اسیدی شبانه”
ترشح اسید شبانه عامل اصلی پاتوفیزیولوژیک در تداوم زخمهای اثنیعشر است.
۳.۱. پروفایل ۲۴ ساعته اسید در DU
در بیماران DU، ریتم سیرکادین ترشح اسید حفظ میشود اما دامنه آن (ترشح پایه یا BAO) ۲ تا ۳ برابر افراد سالم است.
۳.۲. فرار اسیدی شبانه (Nocturnal Acid Breakthrough – NAB)
NAB به افت pH معده به زیر ۴ برای بیش از ۶۰ دقیقه در طول شب اطلاق میشود، حتی با مصرف داروهای PPI. این پدیده به دلیل نیمهعمر کوتاه PPI و افزایش تون عصب واگ در شب رخ میدهد. اسید ترشح شده در شب وارد دوازدهه خالی (بدون بافر غذایی) شده و به مخاط آسیب میزند. کنترل NAB برای بهبود زخم حیاتی است.
فصل چهارم: تمایز بالینی و پروفایل علائم (زخم معده در برابر اثنیعشر)
درک پاتوفیزیولوژی امکان تشخیص افتراقی دقیق را فراهم میکند.
| ویژگی | زخم اثنیعشر (DU) | زخم معده (GU) | مکانیسم پاتوفیزیولوژیک |
|---|---|---|---|
| الگوی زمانی درد | ۲ تا ۳ ساعت بعد از غذا | بلافاصله یا ۳۰-۶۰ دقیقه بعد | زمان تخلیه معده vs تماس مستقیم غذا |
| تأثیر غذا | تسکیندهنده | تشدیدکننده | اثر بافری غذا در DU vs اتساع معده در GU |
| درد شبانه | بسیار شایع (بیدارکننده) | کمتر شایع | اوج اسید شبانه و معده خالی |
| تغییرات وزن | افزایش وزن | کاهش وزن (ترس از غذا) |
۴.۱. تحلیل مکانیسم “تسکین با غذا” در زخم اثنیعشر
پدیده “Hunger Pain” در DU بر سه پایه استوار است:
- ظرفیت بافری شیمیایی: غذا پروتونهای آزاد را جذب کرده و pH را موقتاً افزایش میدهد.
- دینامیک اسفنکتر پیلور: بسته شدن پیلور پس از غذا مانع از پاشش اسید به دوازدهه میشود.
- فاز بازگشت درد: پس از تخلیه معده (۱.۵ تا ۳ ساعت بعد)، اسید “خالص” تحریک شده وارد دوازدهه شده و درد باز میگردد.
فصل پنجم: عوارض حیاتی – پرفوراسیون (Perforation) و سندرم والنتینو
پرفوراسیون یک اورژانس جراحی است که زمانی رخ میدهد که زخم از تمام لایههای دیواره عبور کند.
۵.۱. آناتومی پرفوراسیون و پاتوفیزیولوژی پریتونیت
اکثریت پرفوراسیونها (۶۰٪) در دیواره قدامی حباب دوازدهه رخ میدهند، زیرا این دیواره آزاد است و به حفره صفاق باز میشود. نشت شیره معده باعث پریتونیت شیمیایی شدید (درد ناگهانی خنجری و شکم تختهای) میشود.
۵.۲. سندرم والنتینو (Valentino’s Syndrome): تقلیدگر بزرگ
تعریف: درد در ربع تحتانی راست شکم (شبیه آپاندیسیت) ناشی از پرفوراسیون زخم پپتیک.
مکانیسم: مایعات نشت کرده از دوازدهه از طریق “ناودان پاراکولیک راست” به سمت پایین هدایت شده و در حفره ایلیاک راست تجمع مییابند و باعث التهاب موضعی روی آپاندیس میشوند.
فصل ششم: عوارض حیاتی – خونریزی (Hemorrhage) و آناتومی عروقی
خونریزی شایعترین عارضه است و به آناتومی عروقی ناحیه خلفی دوازدهه وابسته است.
۶.۱. قانون “خلفی خونریزی میکند”
برخلاف پرفوراسیون (دیواره قدامی)، خونریزیهای عظیم عمدتاً از زخمهای دیواره خلفی منشأ میگیرند.
۶.۲. نقش کلیدی شریان گاسترودوodenal (GDA)
شریان گاسترودوodenal مستقیماً از پشت قسمت اول دوازدهه عبور میکند. زخمهای نفوذکننده خلفی باعث فرسایش دیواره این شریان بزرگ شده و منجر به خونریزی جهنده و شوک هیپوولمیک میشوند.
فصل هفتم: اتیولوژیهای H. pylori منفی و زخمهای ایدیوپاتیک
با کاهش شیوع H. pylori، نسبت زخمهای غیرمرتبط با این باکتری رو به افزایش است.
۷.۱. زخمهای ناشی از NSAID
مصرف NSAIDها (مانند آسپرین، ایبوپروفن) دومین علت شایع است. این داروها با مهار COX-1، تولید پروستاگلاندینهای محافظ (مسئول ترشح موکوس و بیکربنات) را متوقف میکنند و سد دفاعی مخاط را تضعیف مینمایند.
۷.۲. زخمهای ایدیوپاتیک واقعی
حدود ۲۰٪ زخمها بدون عفونت یا مصرف دارو هستند. علل احتمالی شامل تخلیه سریع معده، استرس اکسیداتیو و ایسکمی مخاطی است. این زخمها نرخ عود و مرگومیر بالاتری دارند.
نتیجهگیری نهایی
تحلیل جامع نشان میدهد که زخم اثنیعشر حاصل برهمکنش پیچیده میان عفونت H. pylori (التهاب آنترال و سرکوب سلول D) و پاسخهای فیزیولوژیک میزبان (هایپرگاسترینمی و متاپلازی معده) است. تفاوتهای بارز بالینی با زخم معده ریشه در دینامیک ترشحی دارد. درک آناتومی (قدامی vs خلفی) پیشبینیکننده نوع عوارض مرگبار است.
| مکانیسم آسیب | زخم اثنیعشر (DU) | زخم معده (GU) |
|---|---|---|
| نقش اسید | اولیه و حیاتی (Hyperchlorhydria) | ثانویه (Normo/Hypochlorhydria) |
| محل التهاب | آنتروم (Antral-predominant) | کورپوس یا پانگاستریت |
| سلولهای پاریتال | هایپرپلازی | آتروفی |
| دفاع مخاطی | کاهش بی کربنات دوازدهه | نقص در سد موکوسی |
| محل آناتومیک | عارضه غالب | تظاهر بالینی ویژه |
|---|---|---|
| دیواره قدامی | پرفوراسیون | پریتونیت شیمیایی، سندرم والنتینو |
| دیواره خلفی | خونریزی | شوک هیپوولمیک (آسیب به شریان GDA) |
| دیواره خلفی | نفوذ (Penetration) | درد ارجاعی به کمر، پانکراتیت |
| کانال پیلور | انسداد | استفراغ جهنده، آلکالوز متابولیک |
بازبینی توسط متخصص
بازبین علمی این مقاله
آیا درد معده شما نگرانکننده است؟
زخمهای پپتیک میتوانند عوارض جدی داشته باشند. اگر علائمی مانند درد شدید شکم، استفراغ خونی یا مدفوع تیره دارید، یا سابقه خانوادگی مشکلات گوارشی دارید، تیم ما آماده ارائه مشاوره تخصصی است.
دریافت مشاوره ژنتیک