گزارش جامع تحقیقاتی: پاتوفیزیولوژی تکاملی، محرکهای متابولیک و تظاهرات بالینی آدنوکارسینوم مری
تحلیلی بر تغییر چشمانداز بدخیمیهای مری و مکانیسمهای مولکولی
۱. مقدمه: تغییر چشمانداز بدخیمیهای مری
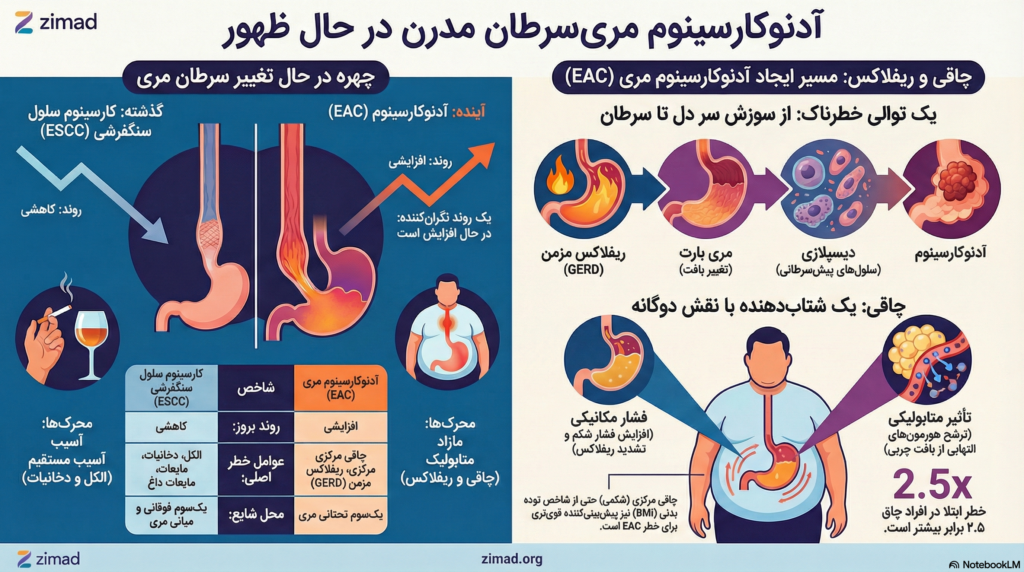
اپیدمیولوژی سرطان مری در نیم قرن گذشته در جهان غرب دستخوش تغییری عمیق و بنیادین شده است که یکی از شدیدترین تغییرات در الگوهای سرطان انسانی در تاریخ پزشکی مدرن محسوب میشود. از لحاظ تاریخی، کارسینوم سلول سنگفرشی (ESCC) زیرگروه بافتشناسی غالب بود که عمدتاً ناشی از اثرات سمی هم افزایی تنباکو و مصرف الکل ایجاد میشد. با این حال، در حالی که بروز ESCC در بسیاری از کشورهای توسعهیافته تثبیت شده یا کاهش یافته است، بروز آدنوکارسینوم مری (EAC) به صورت تصاعدی افزایش یافته و در چهار دهه گذشته در ایالات متحده و اروپا بیش از ۷۰۰ درصد رشد داشته است.
این وارونگی اپیدمیولوژیک نشاندهنده تغییر اساسی در محرکهای سرطانزای مؤثر بر جمعیت است. در حالی که ESCC اغلب بیماری مرتبط با محرومیتهای اجتماعی-اقتصادی و آسیبهای محیطی مستقیم به مخاط سنگفرشی است، EAC به طور فزایندهای به عنوان بیماری ناشی از مازاد متابولیک، التهاب مزمن و “تغذیه بیش از حد” (Over-nutrition) شناخته میشود. این بدخیمی تقریباً منحصراً از زمینه مری بارت (BE) ناشی میشود که خود یک سازگاری متاپلاستیک به بیماری ریفلاکس معده به مری (GERD) مزمن است.
درک EAC نیازمند یک تحلیل چندبعدی است که از تکامل مولکولی پوشش داخلی مری، اثرات غدد درونریز سیستمیک چاقی احشایی، و نارسایی بیومکانیکی مجرای مری که منجر به تظاهرات بالینی ویرانگر آن میشود، عبور کند. این گزارش بررسی دقیقی از این حوزهها ارائه میدهد و پیشرفت از ریفلاکس خوشخیم به کارسینوم تهاجمی، نقش منحصر به فرد و قدرتمند چاقی به عنوان یک عامل خطر اختصاصی برای آدنوکارسینوم (در تضاد مستقیم با کارسینوم سلول سنگفرشی)، و مبانی فیزیولوژیک علائم هشداردهندهای که پیشدرآمد این بدخیمی تهاجمی هستند را تحلیل میکند.
۲. پاتوژنز پیشرفت: از GERD مزمن تا آدنوکارسینوم
توسعه آدنوکارسینوم مری یک رویداد ناگهانی نیست، بلکه نقطه اوج یک توالی طولانی و چند مرحلهای از آسیب بافتی، التهاب، ناپایداری ژنتیکی و تغییرات مورفولوژیک است. این توالی که اغلب “آبشار کورئا در مری” نامیده میشود، از GERD مزمن به مری بارت (متاپلازی)، سپس به دیسپلازی درجه پایین، دیسپلازی درجه بالا و در نهایت آدنوکارسینوم تهاجمی حرکت میکند.
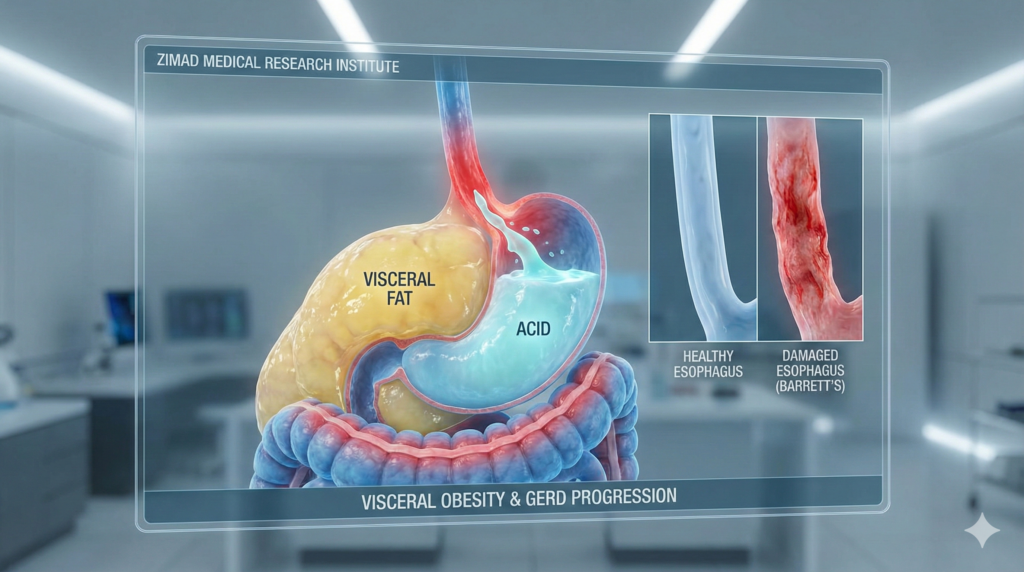
۲.۱ توهین اولیه: بیماری ریفلاکس معده به مری (GERD)
GERD بدون شک عامل خطر اولیه برای توسعه مری بارت است. اپیتلیوم سنگفرشی مری به لحاظ تکاملی برای تحمل اصطکاک مکانیکی طراحی شده است، اما برای مقاومت در برابر خوردگی شیمیایی مجهز نیست. اسفنکتر تحتانی مری (LES) معمولاً به عنوان یک سد عمل میکند؛ با این حال، در بیماران مبتلا به GERD، فشار پایین LES یا شل شدنهای گذرای آن، اجازه میدهد تا محتویات معده به مری دیستال بازگردد.
۲.۱.۱ سمیت هم افزایی اسید و صفرا
در حالی که اسید معده شناختهشدهترین جزء ریفلاکس است، تحقیقات نشان میدهد که اسید به تنهایی ممکن است برای پیش بردن کامل پیشرفت سرطانزا کافی نباشد. اسیدهای صفراوی نقش حیاتی و شاید غالبی در تغییر نئوپلاستیک ایفا میکنند.
- فاکتور صفرا: شواهد آندوسکوپیک ریفلاکس صفرا به عنوان قویترین عامل مستقل مرتبط با مری بارت شناسایی شده است (OR: ۵.۶۵).
- مکانیسم مولکولی آسیب صفرا: اسیدهای صفراوی در pH اسیدی غیر یونیزه میشوند و آزادانه از غشای سلولی عبور میکنند. این امر باعث آسیب میتوکندریایی، تولید ROS و شکستهای DNA میشود. علاوه بر این، اسیدهای صفراوی مسیر NF-κB را فعال میکنند و فاکتور رونویسی CDX2 (تنظیمکننده تمایز روده) را افزایش میدهند.
۲.۲ پاسخ انطباقی: مری بارت (متاپلازی)
مری بارت (BE) به عنوان جایگزینی اپیتلیوم سنگفرشی مطبق با یک لایه اپیتلیوم استوانهای حاوی سلولهای جامی (متاپلازی رودهای) تعریف میشود. این پدیده اساساً یک مکانیسم بقا است؛ سلولهای استوانهای نسبت به آسیب اسید-پپسین مقاومتر هستند، اما این مزیت بقا به قیمت پتانسیل بدخیمی تمام میشود.
۲.۲.۱ تئوریهای منشاء سلولی
فرضیات متعددی برای منشاء سلولی متاپلازی بارت وجود دارد:
- تمایز انتقالی (Transdifferentiation): تبدیل مستقیم سلولهای سنگفرشی به استوانهای از طریق برنامهریزی مجدد ماشین رونویسی (کاهش p63/SOX2 و افزایش CDX1/CDX2).
- مجاری غدد زیر مخاطی: سلولهای بنیادی ساکن در غدد زیر مخاطی که برای ترمیم به سطح مهاجرت میکنند اما در محیط اسیدی به فنوتیپ استوانهای تمایز مییابند.
- سلولهای بنیادی کاردیای معده: مهاجرت سلولها از محل اتصال معده به مری به سمت بالا.
۲.۳ پیشرفت بدخیم: دیسپلازی به آدنوکارسینوم
پس از استقرار، BE به عنوان یک “میدان سرطانی شدن” عمل میکند. پیشرفت به آدنوکارسینوم ناشی از انباشت ضربات ژنتیکی در زمینهای از ناپایداری ژنومی است.
- جهش TP53: از دست دادن عملکرد p53 (“نگهبان ژنوم”) رویداد حیاتی است که به سلولهای آسیبدیده اجازه بقا و تکثیر میدهد.
- ریزمحیط و استرس اکسیداتیو: محیط التهابی مزمن (سیتوکینهای TNF-α, IL-6) و استرس اکسیداتیو (افزایش PARP-1) سوخت این پیشرفت را تامین میکنند.
۳. چاقی: محرک سرطانزای منحصر به فرد آدنوکارسینوم
در میان تمام عوامل خطر سرطان مری، چاقی چشمگیرترین دوگانگی را ارائه میدهد. چاقی یک عامل خطر قوی و وابسته به دوز برای آدنوکارسینوم مری (EAC) است، اما ارتباطی با کارسینوم سلول سنگفرشی مری (ESCC) ندارد.
۳.۱ پارادوکس چاقی: EAC در مقابل ESCC
| ویژگی مقایسهای | آدنوکارسینوم مری (EAC) | کارسینوم سلول سنگفرشی (ESCC) |
|---|---|---|
| تأثیر BMI بالا (≥35) | افزایش خطر ۲.۵ برابری | کاهش خطر تا ۷۰٪ |
| نوع چاقی مؤثر | چاقی احشایی (شکمی) | ارتباط ضعیف یا معکوس |
| وابستگی به دوز | افزایش پیشرونده خطر | بدون الگوی خطی افزایشی |
| محرک متابولیک | لپتین، انسولین، التهاب سیستمیک | مسیر Nrf2، عوامل محیطی (الکل/سیگار) |
۳.۲ چاقی احشایی: “سیب” در برابر “گلابی”
توزیع چربی حیاتی است. چاقی احشایی (چربی مرکزی/شکمی) پیشبینیکننده قویتری برای خطر EAC است. غلبه مردان در آمار EAC (۶ برابر زنان) تا حدی با تمایل مردان به انباشت چربی احشایی (آندروئید) توضیح داده میشود که از نظر متابولیکی فعال است.
۳.۳ مکانیسمهای سرطانزایی ناشی از چاقی
چاقی از طریق دو مسیر متمایز EAC را ترویج میدهد:
۳.۳.۱ مسیر مکانیکی: “مولد ریفلاکس”
چربی اضافی شکمی فشار داخل معده را افزایش میدهد و بر فشار اسفنکتر (LES) غلبه کرده، محتویات معده را به مری میراند. همچنین، چاقی با توسعه فتق هیاتال مرتبط است که سد ضد ریفلاکس را از هم میپاشد.
۳.۳.۲ مسیر متابولیک: “چربی به عنوان غده درونریز”
بافت چربی احشایی آدیپوکینها را ترشح میکند که محیطی تومورزا ایجاد میکنند.
- لپتین (مهاجم): سطح آن در چاقی بالا میرود. لپتین تکثیر سلولی را ترویج کرده و آپوپتوز را مهار میکند (مسیر JAK2/STAT3).
- آدیپونکتین (محافظ): سطح آن در چاقی کاهش مییابد. کمبود آدیپونکتین “ترمز” طبیعی رشد سلولی را حذف میکند.
- انسولین و IGF-1: چاقی محرک مقاومت به انسولین است. انسولین و IGF-1 میتوژنهای قوی هستند که تکثیر سلولهای سرطانی را تحریک میکنند.
- التهاب: چربی احشایی سیتوکینهای التهابی (IL-6, TNF-α) ترشح میکند که التهاب مزمن سیستمیک را ایجاد میکند.
۴. تظاهرات بالینی و علائم هشداردهنده
آدنوکارسینوم مری به طور بدنامی موذی است. مری قابلیت اتساع دارد، بنابراین تومورها میتوانند قبل از ایجاد علائم انسدادی به اندازههای قابل توجهی رشد کنند.
۴.۱ دیسفاژی پیشرونده: علامت اصلی
دیسفاژی (دشواری در بلع) شایعترین علامت است. این علامت معمولاً پیشرونده است؛ ابتدا با جامدات بزرگ و سپس با مایعات مشکل ایجاد میشود.
بیومکانیک انسداد: دیسفاژی معمولاً زمانی آشکار میشود که قطر لومن مری به کمتر از ۱۳ میلیمتر کاهش یابد (انسداد بیش از ۵۰-۶۰ درصد). بیماران اغلب با جویدن طولانیتر یا تغییر رژیم غذایی به طور ناخودآگاه با این تنگی سازگار میشوند که منجر به تأخیر در تشخیص میشود.
۴.۲ اودینوفاژی: اهمیت درد
اودینوفاژی (بلع دردناک) در زمینه سرطان مری معمولاً نشاندهنده زخم شدن سطح تومور یا تهاجم عمیق به بافتهای اطراف (مدیاستن، پلورا) است. درد شدید و مداوم هنگام بلع یک علامت شوم است که اغلب نشاندهنده بیماری مرحله پیشرفته (T4) میباشد.
۴.۳ علائم عصبی-آناتومیک پیشرفته
- گرفتگی صدا: تهاجم تومور یا متاستاز لنفاوی میتواند عصب حنجرهای راجعه چپ را درگیر کند و منجر به فلج تار صوتی شود.
- سکسکههای مداوم: درگیری عصب فرنیک یا دیافراگم توسط تومور میتواند باعث سکسکههای مقاوم شود.
۴.۴ علائم سیستمیک و متابولیک
کاهش وزن ناخواسته چندعاملی است و ناشی از “گرسنگی مکانیکی” (دیسفاژی)، “کاشکسی سرطانی” (سیتوکینهای التهابی) و کمخونی فقر آهن (خونریزی مزمن) میباشد.
۵. چارچوبهای تشخیص و نظارت
با توجه به پیشآگهی ناگوار EAC علامتدار، تمرکز بالینی به سمت غربالگری و نظارت بر ضایعه پیشساز، یعنی مری بارت، تغییر یافته است.
۵.۱ دستورالعملهای غربالگری
کالج گوارش آمریکا (ACG) غربالگری BE را در مردان با علائم مزمن (>5 سال) یا مکرر GERD که دارای عوامل خطر اضافی (سن >50، نژاد سفیدپوست، چاقی مرکزی، سیگار، سابقه خانوادگی) هستند، توصیه میکند.
۵.۲ نظارت بر مری بارت
پس از تشخیص BE، آندوسکوپی نظارتی انجام میشود:
- بدون دیسپلازی: هر ۳ تا ۵ سال.
- دیسپلازی درجه پایین (LGD): تایید توسط پاتولوژیست دوم و سپس درمان ریشهکنی (ابلیشن) یا نظارت دقیق (هر ۱۲ ماه).
- دیسپلازی درجه بالا (HGD) / کارسینوم: اندیکاسیون برای مداخله فوری (EMR یا RFA).
۵.۳ محدودیتهای عملکرد فعلی
با وجود دستورالعملها، اکثر موارد EAC در بیمارانی تشخیص داده میشوند که بدون تشخیص قبلی BE هستند. این “شکست غربالگری” نیاز به روشهای غیرتهاجمی بهتر و آگاهی بیشتر نسبت به علائم ظریف را برجسته میکند.
۶. نتیجهگیری
آدنوکارسینوم مری یک مدل پارادایماتیک از بدخیمی مدرن است: یک سرطان التهابی که توسط عوامل سبک زندگی (چاقی)، آسیب مزمن بافتی (ریفلاکس) و سازگاریهای مولکولی خاص (متاپلازی) هدایت میشود.
پیشرفت از GERD به BE و سپس EAC یک “طوفان کامل” بیولوژیکی است که در آن صفرا و اسید با هم همکاری میکنند. چاقی به عنوان یک شتابدهنده منحصر به فرد عمل میکند، هم از طریق نیروی مکانیکی و هم از طریق سوخت هورمونی. تشخیص منظومه عوامل خطر – چاقی مرکزی، GERD مزمن و جنسیت مذکر – بهترین ابزار پزشک برای مداخله زود هنگام قبل از شروع علائم هشداردهنده شوم دیسفاژی است.
بازبینی توسط متخصص
بازبین علمی این مقاله
آیا سابقه خانوادگی سرطان مری دارید؟
درک زمینه ژنتیکی و عوامل خطر خانوادگی در سرطان مری و مری بارت میتواند در تشخیص زودهنگام و پیشگیری موثر باشد. تیم ما آماده ارائه مشاوره تخصصی برای ارزیابی ریسک شماست.
دریافت مشاوره ژنتیک