
آهن
نقشه یادگیری این مقاله
۱. پادکست: برای درک کلی، ابتدا به پادکست گوش دهید.
۲. ویدیو: ویدیو آموزشی را برای یادگیری عمیق مشاهده کنید.
۳. مطالعه متن: در نهایت، متن مقاله را به عنوان منبع جامع مرور کنید.
مشاهده ویدیو در آپارات
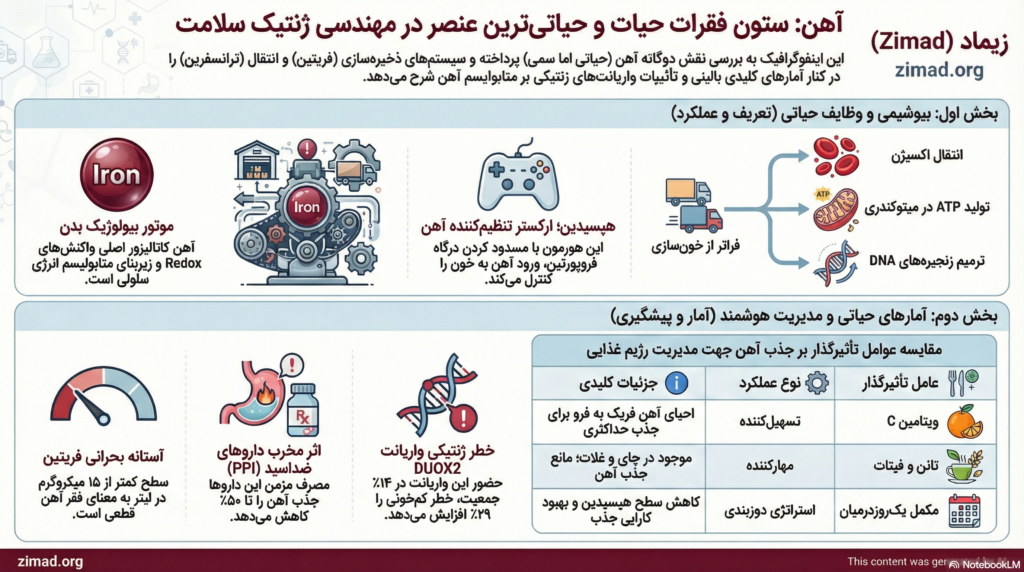
آهن: ستون فقرات حیات؛ تحلیل جامع از بیوشیمی سلولی تا مهندسی ژنتیک سلامت
سفری علمی در مکانیسمهای هومئوستاز، جذب و تنظیم ژنتیکی آهن در بدن انسان
۱. موتور بیولوژیک: تحلیل بیوشیمیایی رفتار آهن
آهن در بیولوژی انسانی عنصری استراتژیک و منحصربهفرد است؛ مادهای که به دلیل ماهیت دووجهی خود، هم برای حیات سلولی «حیاتی» و هم در صورت عدم مدیریت صحیح، «سمی» است. توانایی استثنایی این عنصر در تغییر حالت اکسیداسیون بین دو فرم فِرو (Fe2+) و فِریک (Fe3+)، به بدن اجازه میدهد تا الکترونها را در فرآیندهای حیاتی جابجا کند. این ویژگی، آهن را به کاتالیزور اصلی واکنشهای اکسایش-کاهش (Redox) تبدیل میکند که زیربنای متابولیسم انرژی است.
برای مدیریت این قدرت واکنشپذیری بالا و جلوگیری از آسیبهای اکسیداتیو، بدن از یک سیستم لجستیک هوشمند بهره میبرد: فریتین به عنوان «انبار» اصلی، آهن را در داخل سلولها به شکلی ایمن ذخیره میکند، در حالی که ترانسفرین مانند «کامیونهای توزیع»، وظیفه انتقال آهن در پلاسما و تحویل آن به بافتهای نیازمند را بر عهده دارد. پایداری بیوشیمیایی پلاسما در گرو هماهنگی دقیق بین این انبارها و ناوگان حملونقل است تا از حضور آهن آزاد و مخرب در خون جلوگیری شود.
نکته پژوهشگر (Researcher’s Note):
هپسیدین (Hepcidin) به عنوان «کنترلچی اصلی» یا تنظیمکننده مرکزی ارکستر آهن عمل میکند. این هورمون با مسدود کردن و تخریب فروپورتین (تنها درگاه خروجی آهن از سلول)، ورود آهن از روده به خون و آزادسازی آن از ذخایر ماکروفاژها را متوقف میکند. جالب اینجاست که در شرایط چاقی و التهاب مزمن، سطح هپسیدین به طور پاتولوژیک افزایش مییابد که منجر به کاهش جذب آهن و بروز فقر آهن عملکردی، علیرغم مصرف کافی، میگردد.
۲. سبد وظایف حیاتی: فیزیولوژی آهن در بدن
نقش آهن در بدن بسیار فراتر از تصور سنتی «خونسازی» است؛ این عنصر در واقع سوخت اصلی بقای سلولی محسوب میشود.
- انتقال اکسیژن: آهن قلب تپنده هموگلوبین در گلبولهای قرمز (برای انتقال اکسیژن) و میوگلوبین در عضلات (برای ذخیره اکسیژن جهت فعالیتهای انقباضی) است.
- تولید انرژی و ترمیم: آهن در زنجیره انتقال الکترون میتوکندری برای تولید ATP ضروری است. همچنین، این عنصر نقشی کلیدی در سنتز و ترمیم زنجیرههای DNA ایفا میکند.
- عملکرد شناختی: آهن در سنتز انتقالدهندههای عصبی (نروترانسمیترها) نقش ساختاری دارد.
نکته پژوهشگر (Researcher’s Note):
بسیاری از مراجعین با شکایت از «مه مغزی» (Brain Fog) مراجعه میکنند، در حالی که هموگلوبین آنها لزوماً در محدوده آنمیک نیست. حقیقت این است که حتی افت جزئی در ذخایر آهن، پیش از بروز کمخونی، عملکرد عصبی و سنتز نروترانسمیترها را مختل کرده و منجر به اختلال در تمرکز و حافظه میشود.
۳. توازن «گلدیلاک»: مرز ظریف میان کمبود و سمیت
بدن انسان همواره در تلاش است تا در محدوده «گلدیلاک» (نه خیلی زیاد و نه خیلی کم) باقی بماند. بر اساس دادههای بالینی، آستانه فریتین کمتر از ۱۵ میکروگرم در لیتر نشاندهنده فقر آهن قطعی است، در حالی که سطح کمتر از ۳۰ میکروگرم در لیتر با احتمال پیشتست بالا، قویاً نشاندهنده کمبود ذخایر است.
- فقر آهن: باید میان کمخونی فقر آهن (IDA) و فقر آهن غیرآنمیک تفاوت قائل شد. علائمی نظیر خستگی مفرط، ریزش مو و پیکا (اشتهای کاذب به مواد غیرخوراکی مانند یخ یا خاک) از پیامدهای این وضعیت هستند.
- اضافه بار آهن (سمیت): در بیماریهایی مانند هموکروماتوز، تجمع بیش از حد آهن رخ میدهد. آهن «آزاد» از طریق واکنش فنتون (Fenton Reaction) باعث تولید رادیکالهای آزاد سمی میشود که نتیجه آن آسیب اکسیداتیو شدید به کبد و قلب است.
نکته پژوهشگر (Researcher’s Note):
پدیدهای به نام «کمخونی عملکردی» در زمان التهاب یا عفونت رخ میدهد؛ جایی که بدن آهن را در ماکروفاژها «زندانی» میکند تا از دسترس پاتوژنها خارج شود. در این حالت، فریتین ممکن است نرمال یا حتی بالا به نظر برسد، اما آهن در دسترس برای ساخت گلبولهای قرمز (TSAT) به شدت پایین است.
۴. بشقاب غذا و درگاه جذب: رژیم غذایی و سینرژیستها
جذب آهن یک فرآیند پیچیده است که تحت تأثیر مستقیم انتخابهای تغذیهای قرار دارد. آهن هِم (Heme) در منابع حیوانی جذب بسیار بالاتری نسبت به آهن غیرهِم (گیاهی) دارد.
- تسهیلکنندهها: ویتامین C (اسید اسکوربیک) با احیای آهن فریک به فرو، جذب را به شدت افزایش میدهد.
- مهارکنندهها: فیتاتها (در غلات)، تاننها (در چای/قهوه) و اگزالاتها (موجود در اسفناج) جذب آهن را مهار میکنند. برخلاف تصور عامه، اسفناج منبع ایدهآلی برای تامین آهن نیست مگر آنکه با ویتامین C همراه شود.
- استراتژی دوزبندی متناوب (Alternate Day Dosing): یافتههای نوین نشان میدهد مصرف دوزهای بالای آهن (بیش از ۶۰ میلیگرم) باعث افزایش سطح هپسیدین تا ۲۴ ساعت میشود که جذب دوز بعدی را مسدود میکند. بنابراین، مصرف یکروزدرمیان مکمل آهن، کارایی جذب را افزایش و عوارض گوارشی را کاهش میدهد.
نکته پژوهشگر (Researcher’s Note):
اسید معده برای حلالیت آهن حیاتی است. استفاده مزمن از داروهای ضداسید معده مانند PPIها (امپرازول و غیره) با قلیایی کردن محیط معده، جذب آهن را متوقف کرده و یکی از دلایل اصلی فقر آهن مقاوم به درمان است.
۵. نقشه ژنتیک: شخصیسازی سلامت بر اساس واریانتها
انقلاب مطالعات GWAS نشان داده است که متابولیسم آهن در هر فرد، تابع یک «کد ژنتیکی» اختصاصی است:
- ژن DUOX2: واریانت p.His678Arg در ۱۴٪ جمعیت حضور دارد و خطر ابتلا به کمخونی را تا ۲۹ درصد افزایش میدهد.
- واریانت HBS1L-MYB: این یک «شمشیر دو لبه» ژنتیکی است؛ به طور همزمان خطر اضافه بار آهن را افزایش و خطر کمخونی فقر آهن را کاهش میدهد.
- ژن STAB1: واریانتهای این ژن (نظیر p.Glu117Ter) قویترین تأثیر را بر افزایش فریتین دارند (0.35 SD)، اما الگویی پارادوکسیکال ایجاد میکنند: فریتین بالا همزمان با هموگلوبین پایین، که نشاندهنده شکست در بازیافت آهن از ذخایر است.
- ژن F5 (Factor V Leiden – rs6025): این واریانت در زنان اثری محافظتی در برابر فقر آهن و خونریزی شدید قاعدگی (Menorrhagia) دارد.
- حذف SLC11A2: کشف یک حذف ۳.۵ کیلوبازی در ایسلندیها نشان داد که حذف رونوشت +IRE منجر به نوعی فقر آهن موروثی مغلوب (IDA) میشود که با کاهش شدید جذب دئودنال همراه است.
نکته پژوهشگر (Researcher’s Note):
ژنتیک به ما میگوید چرا برخی افراد با رژیم گیاهخواری دچار کمخونی شدید میشوند (واریانت TMPRSS6) و برخی دیگر علیرغم قاعدگیهای سنگین، ذخایر آهن خود را حفظ میکنند (واریانت F5). این یعنی درمان باید «شخصیسازی شده» باشد.
۶. جدول خلاصه اقدام سریع (Quick-Action Summary)
| هدف | انتخاب غذایی/اقدام کلیدی | زمانبندی طلایی | ملاحظه ژنتیکی/بالینی |
|---|---|---|---|
| بیشینهسازی جذب | ترکیب منابع هِم با ویتامین C | مصرف مکمل به صورت یکروزدرمیان | اگر واریانت DUOX2 دارید، پایش سالانه فریتین الزامی است. |
| رفع مهارکنندهها | کاهش مصرف اسفناج پخته به تنهایی | پرهیز از چای، قهوه و کلسیم تا ۲ ساعت پس از غذا | مصرف مزمن PPIها (ضد اسید) جذب را تا ۵۰٪ کاهش میدهد. |
| پیشگیری از خستگی | تمرکز بر پروتئینهای حیوانی و جگر | افزایش دریافت در دوران قاعدگی | واریانت F5 (Factor V Leiden) محافظ در برابر فقر آهن است. |
| مدیریت بازیافت آهن | پایش سطح التهاب (CRP) | بررسی عملکرد کبد و طحال | در صورت الگوی فریتین بالا/هموگلوبین پایین، ژن STAB1 را بررسی کنید. |
| کنترل سمیت | محدود کردن آهن هِم در موارد خاص | تست ژنتیک در صورت سابقه خانوادگی | واریانت HBS1L-MYB مستعدکننده به اضافه بار آهن است. |
این تحلیل جامع نشان میدهد که مدیریت آهن دیگر یک رویکرد عمومی نیست، بلکه باید بر اساس بیوشیمی فردی، شاخصهای بالینی (فریتین ۱۵/۳۰) و نقشهبرداری دقیق ژنتیکی انجام پذیرد.
مطالعه بیشتر درباره مخازن و ناقلهای آهن
برای درک عمیقتر مکانیسمهای ذخیرهسازی و انتقال آهن در بدن، مقالات تخصصی زیر را مطالعه کنید:
بازبینی علمی و تخصصی
دکتر محمدرضا قاسمی
متخصص ژنتیک پزشکی و بنیانگذار زیماد
باربد الهوئی
کارشناس تغذیه و رژیمدرمانی
آیا متابولیسم آهن در بدن شما به درستی کار میکند؟
تفاوتهای ژنتیکی میتوانند تأثیر مستقیمی بر نحوه جذب، ذخیرهسازی و مصرف آهن داشته باشند. برای بررسی دقیق وضعیت ژنتیکی و دریافت برنامه تغذیهای اختصاصی، با ما در تماس باشید.
دریافت مشاوره تخصصی زیماد